
 Пацієнтка Г.І., 64 роки**.
Пацієнтка Г.І., 64 роки**.
Звернулася до лікаря поліклініки за місцем проживання зі скаргами на біль у грудній клітці, що часто виникає, задишку під час звичної фізичної активності, як-то прибирання вдома чи піднімання сходами (що змушує робити зупинку вже на 2-му поверсі), сильний головний біль, мерехтіння мушок перед очима, відчуття тривоги (яке може з’являтися навіть від самої думки про наявність серцевих проблем). Самостійно вдома почала вимірювати артеріальний тиск (АТ): практично завжди він у межах 160/90–170/95 мм рт. ст. Відмічає погіршення сну, безсоння вночі та неможливість сконцентрувати увагу вдень. Постійно наявне відчуття швидкої втоми, неспокою, настрій пригнічений. Симптоми турбують впродовж останніх 3 міс.
Після смерті чоловіка почала багато їсти. У раціоні переважно борошняні вироби, картопля, жирна їжа. Впродовж останнього року значно збільшилася маса тіла.
Працює бухгалтером. Спортом не займається, веде малорухливий спосіб життя. Шкідливих звичок не має.
Із сімейного анамнезу відомо, що мати та бабуся страждали на гіпертонічну хворобу та мали надмірну масу тіла.
Об’єктивно:
Маса тіла 100 кг, зріст 165 см, індекс маси тіла 36,7 кг/м2.
Пульс 68 уд./хв, ритмічний.
АТ 163/94–160/93–157/90 мм рт. ст.
Пальпаторно край печінки на 3 см нижче реберної дуги.
Невеликі набряки нижніх 1/3 гомілок.
Електрокардіографія (ЕКГ): неспецифічні зміни сегмента ST та зубця T.
Оцінка за опитувальником здоров’я пацієнта (Patient Health Questionnaire — PHQ-9) — 6 балів; за Госпітальною шкалою тривоги та депресії (Hospital Anxiety and Depression Scale — HADS): депресія — 12, тривога — 8 балів.
Попередній діагноз:
«Есенціальна артеріальна гіпертензія II ступеня, 2-ї(?) стадії, ризик (?). Ішемічна хвороба серця, стабільна стенокардія напруги I(?) функціонального класу. Хронічна серцева недостатність, стадія В(?)С(?), II(?) функціонального класу за NYHA. Ожиріння 2-го ступеня. Порушення вуглеводного обміну(?)».
Який план кардіологічного обстеження можна призначити пацієнтці?
На основі представлених даних попередньо можна говорити про наявну артеріальну гіпертензію (АГ). Під сумнівом питання щодо ішемічної хвороби серця (ІХС) і ступеня серцевої недостатності (СН). З точки зору кардіолога, безумовно, потребується дообстеження пацієнтки (табл. 1).
Таблиця 1. Необхідні та оптимальні обстеження згідно з клінічними рекомендаціями Міжнародного товариства артеріальної гіпертензії (International Society of Hypertension — ISH) 2020 р. [1]
| Обстеження | |
|---|---|
| Необхідні | Оптимальні |
| Анамнез | Додаткові обстеження для виявлення ураження органів-мішеней, супутніх захворювань та вторинної АГ |
| АТ | ЕхоКГ |
| Фактори ризику | Ультразвукове дослідження сонних артерій |
| Симптоми ураження органів-мішеней | Візуалізація ниркових артерій |
| Ознаки, що можуть вказувати на вторинну АГ | Фундоскопія |
| Огляд | КТ/магнітно-резонансна томографія головного мозку |
| Лабораторні обстеження: | Функціональні тести та додаткові обстеження: |
|
|
|
|
| ЕКГ у 12 відведеннях | |
Щодо наявності ІХС є певні питання. Перед тим як встановлювати цей діагноз, слід оцінити ймовірність наявності ІХС за шкалою Європейського товариства кардіології (European Society of Cardiology — ESC), яка враховує стать, вік, типовість/атиповість наявної клінічної симптоматики (у пацієнтки Г.І. вона є неангінозною, нетиповою) (табл. 2). У той самий час останні рекомендації Американської асоціації серця (American Heart Association — AHA) свідчать, що у віковому діапазоні, до якого належить обстежувана пацієнтка, у більшості хворих біль у грудній клітці має некардіальне походження і слід дуже ретельно зважувати стосовно цього діагнозу [3].
Таблиця 2. Передтестова ймовірність обструктивної ІХС у 15 815 симптоматичних пацієнтів залежно від віку, статі та характеру симптомів в об’єднаному аналізі сучасних даних [2]
| Вік, роки | Типова | Атипова | Неангінальна | Задишка | ||||
|---|---|---|---|---|---|---|---|---|
| Чоловіки, % | Жінки, % | Чоловіки, % | Жінки, % | Чоловіки, % | Жінки, % | Чоловіки, % | Жінки, % | |
| 30–39 | 3 | 5 | 4 | 3 | 1 | 1 | 0 | 3 |
| 40–49 | 22 | 10 | 10 | 6 | 3 | 2 | 12 | 3 |
| 50–59 | 32 | 13 | 17 | 6 | 11 | 3 | 20 | 9 |
| 60–69 | 44 | 16 | 26 | 11 | 22 | 6 | 27 | 14 |
| ≥70 | 52 | 27 | 34 | 19 | 24 | 10 | 32 | 12 |
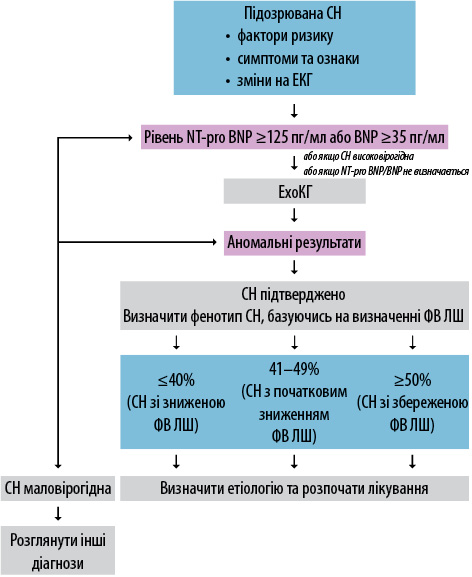
З метою підтвердження/виключення діагнозу ІХС можна використати додаткові дослідження для виявлення ураження коронарних судин або функціональні дослідження для виявлення ішемії (рис. 1). Більшість пацієнтів низького ризику можуть бути направлені на проведення мультиспіральної КТ — і це є дуже потрібним для досліджуваної пацієнтки. Питання щодо задишки, наявності набрякового синдрому потребують підтвердження/виключення СН. За алгоритмом ESC, на тлі обов’язкового врахування симптомів та ознак має бути виконане лабораторне дослідження на вимірювання рівня мозкового натрійуретичного пептиду (NT-pro BNP) та проведення ехоКГ з урахуванням як структурних, так і морфологічних уражень серця (рис. 2).

Яке подальше обстеження може порекомендувати лікар-ендокринолог?
 Порушення вуглеводного обміну, хоча і під питанням, але правильно встановлене в попередньому діагнозі, незважаючи на те, що у пацієнтки не було скарг, які вказували би на підвищення рівня глюкози в крові. Слід зазначити, що сьогодні маємо бути насторожені щодо категорії пацієнтів віком >35 років: усі вони повинні бути обстежені щодо виявлення підвищеного рівня глюкози в крові. У пацієнтки наявне ожиріння 2-го ступеня, що потребує обов’язкового підтвердження/виключення ЦД або переддіабету. Для цього слід перевірити рівень глюкози у плазмі венозної крові натще. Якщо того потребує клінічна ситуація — провести глюкозотолерантний тест із використанням 75 г глюкози або, що простіше, — визначити рівень глікозильованого гемоглобіну.
Порушення вуглеводного обміну, хоча і під питанням, але правильно встановлене в попередньому діагнозі, незважаючи на те, що у пацієнтки не було скарг, які вказували би на підвищення рівня глюкози в крові. Слід зазначити, що сьогодні маємо бути насторожені щодо категорії пацієнтів віком >35 років: усі вони повинні бути обстежені щодо виявлення підвищеного рівня глюкози в крові. У пацієнтки наявне ожиріння 2-го ступеня, що потребує обов’язкового підтвердження/виключення ЦД або переддіабету. Для цього слід перевірити рівень глюкози у плазмі венозної крові натще. Якщо того потребує клінічна ситуація — провести глюкозотолерантний тест із використанням 75 г глюкози або, що простіше, — визначити рівень глікозильованого гемоглобіну.
Слід пам’ятати про фактори ризику ЦД: вік ≥35 років, надмірна маса тіла або ожиріння (індекс маси тіла ≥25 кг/м2), сімейний анамнез ЦД, порушення толерантності до глюкози або порушення глікемії натще в анамнезі, гестаційний ЦД або народження великого плода в анамнезі, АГ, низька фізична активність, рівень холестерину ліпопротеїдів високої щільності ≤0,9 ммоль/л та/або рівень тригліцеридів ≥2,82 ммоль/л, синдром полікістозних яєчників, наявність ССЗ [6].
Як, зі свого боку, лікар-психіатр може прокоментувати стан пацієнтки?
Звертає на себе увагу те, що близько ⅓ скарг пацієнтки пов’язані з її емоційним станом і фобіями. Навіть не маючи жодних соматичних ознак, вона боїться, що в неї є проблеми зі здоров’ям. Лікар поліклініки правий, провівши пацієнтці скринінг стосовно симптомів тривоги та депресії, адже отримані результати вказують на необхідність додаткових обстежень щодо психоемоційного стану хворої.
Серед фізичних проявів тривоги — порушення сну (одна з перших ознак тривожних розладів), прискорене серцебиття, відчуття перебоїв у роботі серця, м’язова слабкість/напруження, швидка втомлюваність, біль за грудниною/у грудях, головний біль, задишка, біль у животі, диспепсія, відсутність апетиту.
Емоційні прояви: «погане» передчуття, страх, порушення концентрації, відчуття напруження, роздратованість, нав’язливе піклування про своє здоров’я, кошмарні сновидіння, відчуття «дежавю».
Страждає й когнітивна сфера: знижується увага, пацієнту важко зосередитися, погіршуються пам’ять, операційні функції (нерішучість, важко визначити пріоритети, важко щось планувати, приймати елементарні рішення), знижується швидкість психомоторних реакцій (загальмованість, вповільнене мовлення, паузи в реченнях).
Змінюється поведінка: хворий намагається уникати ситуацій, що нагадують про стрес, порушуються патерни сну і денного функціонування, звужується соціальне коло, підвищується рухова активність («метушливість», «топтання на місці»).
В обстежуваної пацієнтки відмічено всі прояви тривоги — фізичні, емоційні, когнітивні та поведінкові.
У результаті замикається хибне коло: нелікована тривога провокує розвиток соматичних захворювань (цереброваскулярної патології, ІХС, бронхіальної астми тощо), а наявність останніх — ще більше підсилює тривогу.
План обстеження:
- лабораторне обстеження за протоколом АГ і ЦД;
- визначення рівня тиреотропного гормону;
- загальний аналіз сечі;
- визначення рівня NT-pro BNP;
- ехоКГ з визначенням індексу маси міокарда ЛШ, індексу об’єму лівого передсердя, показників діастолічної функції ЛШ: E, A, E/A, е’, E/е’, швидкості трикуспідальної регургітації, діаметра нижньої порожнистої вени та її спадіння на вдиху;
- мультиспіральна КТ коронарних артерій;
- домашній моніторинг АТ вранці та ввечері за правилами із записом;
- визначення рівня глюкози у плазмі венозної крові, проведення глюкозотолерантного тесту, визначення рівня глікозильованого гемоглобіну;
- визначення альбумінурії, співвідношення альбумін/креатинін;
- електроенцефалографія;
- визначення рівня кортизолу та швидкості його зростання, рівня адреналіну;
- Бостонський тест стресостійкості, індекс адаптації до стресового впливу;
- повторна консультація з результатами через 10–14 днів.
Чи потрібно одразу призначити лікування чи очікувати на результати додаткових досліджень?
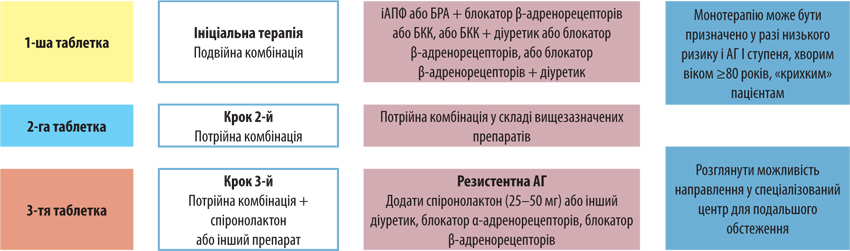
Оскільки пацієнтка має підвищений АТ і підозру на наявну ІХС, слід призначити терапію ще до її повторного візиту. Загалом рекомендації щодо ведення пацієнтів із АГ визначають пріоритетність застосування фіксованих комбінацій (рис. 3). У випадку, що розглядається, має бути призначена подвійна фіксована комбінація БРА + блокатор β-адренорецепторів або БКК. Вбачається за доцільне призначити пацієнтці фіксовану комбінацію на основі валсартану та амлодипіну, аби одразу взяти під контроль АТ. Попередньо у хворої наявні ознаки СН із гіперволемією, тому є обґрунтованим призначення петльових діуретиків задля досягнення умов еуволемії. Оскільки є підозра на ІХС, пацієнтці рекомендовано мати при собі нітрогліцерин, хоча, аналізуючи наявні дані, швидше за все має місце неішемічний компонент стосовно скарг, пов’язаних із больовими відчуттями в ділянці серця.
Аби призначити ефективну антигіперглікемічну терапію, яка впливатиме на віддалені результати та подальший перебіг ЦД або порушення вуглеводного обміну, звичайно, потрібні результати додаткових обстежень. Оскільки є впевненість, що в пацієнтки має місце інсулінорезистентність, можна призначити оригінальний препарат метформіну Глюкофаж XR в дозі 500 мг. Після дообстеження, якщо буде виявлено переддіабет чи ЦД 2-го типу, дозу препарату можна буде дотитрувати.
Щодо порушень психоемоційної сфери: тривожний стан у пацієнтки, ймовірно, виходить за рамки фізіологічної тривоги. Є сенс провести додаткові обстеження для оцінки якості її життя взагалі, використовуючи, наприклад, шкалу оцінювання впливу стресу T.H. Holmes, R.H. Rahe (1967) [5], Бостонський тест стресостійкості або шкалу «Оцінка якості життя» О.С. Чабана. Треба розуміти, що кінцева мета лікування — продовжити життя пацієнтки, покращити її функціональний стан і зробити так, щоб хвороба, яку почали контролювати, не призвела до катастрофічних наслідків.
Початкове лікування:
- валсартан/амлодипін (Діфорс 160) 160/5 мг 1 раз на добу вранці під контролем АТ;
- торасемід 10 мг натще з вимірюванням добової кількості сечі;
- нітрогліцерин під язик при нападі болю за грудниною з оцінкою ефекту;
- дієта з обмеженням солі, вуглеводів, що легко засвоюються, калоражу і розміру порцій. Зменшення маси тіла на 10–15% протягом 6 міс;
- ходьба пішки 150 хв на тиждень, за потреби із зупинками;
- метформін (Глюкофаж XR), починаючи з дози 500 мг під час вечері, після дообстеження дотитрувати дозу до 2000 мг. Корекція лікування — під час наступної консультації;
- психотерапія, антистрес-менеджмент, психоосвіта, за результатами клінічного інтерв’ю та даних психологічного тестування — можливо, адаптогени, антидепресанти 1-ї лінії вибору.
На чому ґрунтується вибір терапії, яку призначено пацієнтці?
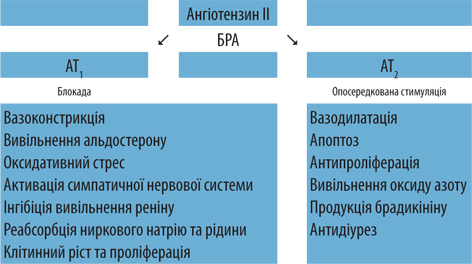
Щодо призначення лікарем-кардіологом комбінації валсартан/амлодипін (Діфорс 160) слід зазначити таке: по-перше, серед блокаторів рецепторів ренін-ангіотензин-альдостеронової системи (РААС) саме сартани мають додаткову перевагу над іАПФ щодо селективної блокади рецепторів ангіотензину І типу та опосередкованої стимуляції рецепторів ангіотензину ІІ типу, що супроводжується додатковими превентивними механізмами (рис. 4). Зокрема, відсутність впливу на брадикінін-калікреїн-кінінову систему зумовлює мінімальну кількість побічних явищ, пов’язаних із призначенням сартанів, що зіставна з плацебо, відсутність ефекту «вислизання» нейрогормональної дії та ін. (табл. 3). Зниження АТ має бути сталим і тривати щонайменше 24 год. Валсартан забезпечує плавне зниження АТ з етапом накопичення без піків, які інколи відмічають як ефект 1-ї дози при застосуванні іАПФ. Слід зазначити, що валсартан має найбільшу доказову базу серед усіх сартанів. Щодо комплаєнсу: якщо порівнювати всі антигіпертензивні препарати, то найменшу кількість відмови виявляють саме при застосуванні валсартану [6]. Крім того, дослідження VALVACE показало, що прийом валсартану знижує частоту рестенозів за рахунок зменшення вираженості запального процесу в атеросклеротичній бляшці [7], що актуально для пацієнтки Г.І. з урахуванням підозри на наявність у неї ІХС. Порівняльна оцінка клінічної ефективності БРА та іАПФ у когортному дослідженні D. Ko та співавторів (2019) у популяції пацієнтів, які перенесли інфаркт міокарда, свідчить, що прийом сартанів асоційований з нижчими показниками несприятливих клінічних серцево-судинних наслідків [8]. По-друге, БКК вважають золотим стандартом у структурі призначення антигіпертензивної терапії, і амлодипін — ключовий і найбільш вивчений представник цього класу як у пацієнтів із АГ та додатковими факторами ризику, так і пацієнтів із ІХС та АГ, в яких отримані переконливі докази щодо зниження ризику тяжких серцево-судинних подій. Саме це стало додатковим важелем при призначенні пацієнтці саме такої антигіпертензивної терапії.
Таблиця 3. Порівняльна характеристика блокаторів РААС
| БРА | іАПФ |
|---|---|
| Максимально повне блокування негативного впливу ангіотензину II | Неповна блокада синтезу ангіотензину II |
| Стимуляція захисних ефектів через АТ2-рецептори | Одночасне зниження захисних ефектів ангіотензину II (через АТ2-рецептори) |
| Відсутність впливу на брадикінін-калікреїн-кінінову систему | Порушення деградації брадикініну (підвищення синтезу простацикліну та оксиду азоту) |
| Низька кількість побічних ефектів, зіставна з плацебо | Кашель в 5–7% випадків |
| Відсутність ефекту «вислизання» нейрогормональної дії | Ефект «вислизання» нейрогормональної дії |
З боку лікаря-ендокринолога вибір молекули валсартану пацієнтці, з урахуванням ймовірної наявності в неї переддіабету або ЦД, зумовлений також тим, що, за даними метааналізу W.J. Elliott, P.M. Meyer (2007), застосування валсартану знижує ризик розвитку ЦД на 43% [9]. Тобто на тлі застосування валсартану пацієнти з наявною інсулінорезистентністю або переддіабетом мають високі шанси уникнути розвитку ЦД, що є значною перевагою для пацієнтів.
Щодо терапії психоемоційних розладів: призначення лікаря-психіатра повинні базуватися не тільки на результатах скринінгових шкал, але й даних клінічного інтерв’ю, адже лікування має бути призначене тільки після встановлення діагнозу. Лікар поліклініки звернув увагу на прояви тривожного синдрому у пацієнтки, але треба розуміти, чи пов’язані наявні емоційні проблеми з соматичною патологією (серцево-судинною, ендокринною), чи це окремий коморбідний розлад? Якщо буде встановлено, що у пацієнтки наявний тривожний розлад (не тривожний синдром), то терапію слід призначати згідно з відповідними клінічними стандартами лікування. У багатьох подібних випадках лікарі-інтерністи самостійно призначають пацієнтам бензодіазепіни — і роблять велику помилку, адже це лише короткофокусна терапія, «швидка допомога», а не лікування. Іншим питанням, на яке треба звернути увагу, є те, що ціла низка лікарських засобів здатна викликати симптоми депресії, особливо при застосуванні протягом тривалого часу. Серед них представники груп антигіпертензивних препаратів, серцевих глікозидів, гормональних препаратів, антиконвульсантів, анальгетиків, нестероїдних протизапальних препаратів, антибіотиків, протитуберкульозних засобів. Тому лише після підтвердження у пацієнтки тривожно-депресивного розладу слід обирати лікування згідно з міжнародними рекомендаціями [10], національним протоколом з урахуванням усіх можливих побічних ефектів. Наприклад, один із найпотужніших антидепресантів, міртазапін, асоційований зі збільшенням маси тіла. Найбільш ефективні та безпечні серед антидепресантів, рекомендованих національним протоколом у якості 1-ї лінії терапії, — агомелатин (якщо не спровокована печінка), есциталопрам, сертралін або препарат подвійної дії венлафаксин.
Тож психотерапія пацієнта з тривожним розладом повинна проводитися на всіх рівнях медичної допомоги: лікар-інтерніст, психолог проводять заходи низької інтенсивності (наприклад психоосвіта, навчання деяким прийомам для швидкого заспокоєння, як-от: «розходження рук», «політ», «сходження рук», «левітація руки» та ін.), а сертифіковані фахівці — психіатр, психотерапевт, медичний психолог — здійснюють втручання високої інтенсивності згідно з протоколами та алгоритмами психотехнік. Потенційно корисні втручання для таких пацієнтів — дозована фізична активність, гігієна сну, тілесна терапія (масаж, акупунктура, м’язова релаксація та ін.), медитація, йога (втручання, які змінюють самоусвідомлення пацієнта як нехворого, формують відповідальне ставлення до свого здоров’я).
Під час візиту через 2 тиж:
- біль у грудній клітці начебто зменшився, нітрогліцерин не приймала;
- набряки зникли;
- АТ протягом останніх 3 днів: 135–139/92–94 мм рт. ст., частота серцевих скорочень 66 уд./хв;
- глюкоза у плазмі венозної крові натще 7,8 ммоль/л, глікозильований гемоглобін 7,4%;
- тиреотропний гормон 1,24 мкОд/мл;
- креатинін 113 мкмоль/л, швидкість клубочкової фільтрації 50 мл/хв/1,73 м², аланінамінотрансфераза 80 Од./л, аспартатамінотрансфераза 50 Од./л;
- загальний холестерин 3,5 ммоль/л, тригліцериди 1,8 ммоль/л, холестерин ліпопротеїдів високої щільності 1,0 ммоль/л, холестерин ліпопротеїдів низької щільності 3,6 ммоль/л;
- мікроальбумінурія 38,4 мг/дл;
- NT-pro BNP 410 пг/мл;
- ехоКГ: ФВ ЛШ 58%, індекс маси міокарда ЛШ 125 г/м2, індекс об’єму лівого передсердя 36 мл/м2, Е/е’ 11 см/с, діаметр нижньої порожнистої вени 22 мм, середній тиск у легеневій артерії 37 мм рт. ст.;
- мультиспіральна КТ коронарних артерій: стеноз правої коронарної артерії й огинаючої гілки лівої коронарної артерії до 50%, індекс Агатсона 90;
- рівень тривоги знизився за суб’єктивною оцінкою і результатами шкалювання.
Остаточний діагноз:
«Гіпертонічна хвороба III стадії, 2-го ступеня, ризик IV. ІХС: атеросклероз коронарних артерій (стеноз правої коронарної артерії й огинаючої гілки лівої коронарної артерії), хронічна СН зі збереженою ФВ ЛШ (58%), стадія С, II функціональний клас за NYHA. Цукровий діабет 2-го типу, вперше виявлений. Хронічна хвороба нирок 3А стадії. Ожиріння 2-го ступеня. Неалкогольна жирова хвороба печінки. Тривожний синдром помірної вираженості».
Чи правильно встановлений остаточний діагноз і як з урахуванням даних додаткових обстежень скоригувати подальше лікування пацієнтки?
Щодо ІХС, наявність якої спочатку ставилася під сумнів, слід зазначити, що дані мультиспіральної КТ свідчать про ймовірну її наявність, але вона не є домінуючою.
З точки зору лікаря-ендокринолога, діагноз встановлений правильно. Звертає на себе увагу, що рівень тиреотропного гормону у пацієнтки нормальний, тобто надмірна маса тіла не зумовлена порушенням функції щитоподібної залози. З урахуванням підтвердженого ЦД 2-го типу, наявності ураження нирок стан такої пацієнтки, безумовно, викликає стурбованість. Успіх лікування в таких випадках залежить від ретельного виконання пацієнтом рекомендацій лікаря. Щодо антигіперглікемічної терапії: пацієнтці вже призначено Глюкофаж XR, адже, за рекомендаціями Американської діабетичної асоціації (American Diabetes Association) 2022 р., препаратом 1-ї лінії у таких пацієнтів є метформін [11]. У пацієнтів високого та дуже високого серцево-судинного ризику можна рекомендувати інгібітори натрійзалежного котранспортера глюкози 2-го типу або агоністи рецепторів глюкагоноподібного пептиду-1. У сучасних настановах зазначено, що метформін кожному пацієнту з ЦД 2-го типу має бути призначено «за замовчуванням».
У пацієнтки наявна інсулінорезистентність: її клітини «голодують», не отримуючи глюкози, тому що вони резистентні до інсуліну, який виділяє підшлункова залоза. Оригінальний метформін Глюкофаж XR знижує вивільнення глюкози в печінці, підсилює використання глюкози м’язами, зменшує всмоктування глюкози в кишечнику, гальмує синтез глюкози з білків та жирів, підвищує чутливість периферичних рецепторів до інсуліну, позитивно впливає на ліпіди крові. Крім того, важливою особливістю препарату є його кардіопротекторна дія, доведена 65-річною історією дослідження цього препарату.
Оригінальний метформін Глюкофаж XR має низку переваг порівняно з генеричними препаратами: абсолютна довіра пацієнтів (за даними опитування, 96,5% пацієнтів надають перевагу оригінальному препарату), кількість побічних ефектів з боку шлунково-кишкового тракту при його застосуванні менша на 53%, кількість випадків діареї — на 77%. До того ж зручність прийому 1 раз на добу підвищує вірогідність того, що пацієнт буде дотримуватися рекомендацій.
Існує міф про те, що у пацієнтів із хронічною хворобою нирок (ХХН) має бути відмінений метформін — це не так. У табл. 4 представлена інформація Управління з контролю за харчовими продуктами та лікарськими засобами США (Food and Drug Administration — FDA) 2016 р., в яких випадках слід залишити, а в яких — відмінити прийом препарату. У цьому разі пацієнтці слід не тільки залишити прийом метформіну, а й дотитрувати дозу до 2000 мг/добу, з подальшим спостереженням за функцією нирок.
Таблиця 4. Застосування метформіну при ХХН
| Швидкість клубочкової фільтрації, мл/хв/1,73 м2 | Дія |
|---|---|
| >60 |
Немає протипоказань з боку нирок до застосування метформіну Щорічний контроль функції нирок |
| <60 і >45 |
Продовжувати застосування Посилити моніторинг функції нирок (кожні 3–6 міс) |
| <45 і >30 |
Метформін призначають з обережністю Застосовують нижчу дозу (наприклад 50% або половину максимальної дози) Ретельно стежать за функцією нирок (кожні 3 міс) |
| <30 | Припиняють прийом метформіну |
Слід пам’ятати про підтверджені в дослідженнях переваги метформіну щодо зниження загальної і серцево-судинної смертності у пацієнтів із ЦД 2-го типу та ХХН. Так, застосування метформіну асоціювалося зі зниженням ризику смерті від усіх причин на 51%, серцево-судинної смерті на 51%, комбінованих серцево-судинних подій на 44% та тяжких захворювань нирок на 33% [12].
Необхідно відзначити виражений нефропротекторний ефект препарату Діфорс 160 за рахунок того, що валсартан знижує ризик ниркових ускладнень на 42,5%. При його застосуванні уповільнюється зниження ниркової функції та зменшується необхідність у нирковозамісній терапії [13].
При призначенні антигіпертензивної терапії у пацієнтів із ХХН та зниженою швидкістю клубочкової фільтрації є важливі відмінності щодо застосування іАПФ і БРА. У даному клінічному випадку немає сумнівів у доцільності призначеної антигіпертензивної терапії. Але щодо застосування, зокрема іАПФ, є певні обмеження. Необхідно враховувати такі важливі параметри, як швидкість клубочкової фільтрації, співвідношення альбумін/креатинін, показник альбумінурії, тому що на них у тому числі ґрунтується вибір антигіпертензивної терапії.
Чи потрібно призначити додаткове лікування пацієнтці з урахуванням даних ліпідного профілю крові?
Наявний ЦД передбачає застосування статинів, більше того — має бути призначений інтенсивний режим статинотерапії. Найбільший ефект виявляє розувастатин (Клівас 20), який пацієнтка має приймати 1 раз на добу. Щодо побоювань деяких лікарів стосовно призначення статинів пацієнтам із ЦД — це досить давно спростований міф, адже насправді у статинів набагато більше переваг, ніж побічних дій. Статини, поряд із антигіпертензивними та антигіперглікемічними препаратами, повинні бути призначені таким пацієнтам в обов’язковому порядку. Це ті препарати, які подовжують життя пацієнтів і знижують ризик серцево-судинних ускладнень.
Також, зважаючи на результати додаткових обстежень, є підґрунтя для призначення пацієнтці антиагрегантної терапії.
Чи потрібна інтенсифікація зниження рівня глюкози в крові за допомогою нових молекул, які знайшли своє місце не тільки в ендокринології, але й кардіології?
Так, пацієнтці можна рекомендувати інгібітори натрійзалежного котранспортера глюкози 2-го типу з метою нефропротекції і досягнення компенсації ЦД, але, оскільки вона має ще й атеросклеротичне захворювання, можна розглянути й агоніст рецепторів глюкагоноподібного пептиду-1 — досить вартісний, але доказовий варіант терапії.
Згідно із сучасними рекомендаціями у пацієнтів високого та дуже високого серцево-судинного ризику, з ХХН або СН відразу на старті можна призначити метформін з інгібітором натрійзалежного котранспортера глюкози 2-го типу. У даному випадку це може бути, наприклад, дапагліфлозин, враховуючи результати дослідження DAPA-CKD [14].
Підсумовуючи, що можна порадити сімейним лікарям, якщо до них на прийом потрапить подібний пацієнт?
1. Слід пам’ятати, що ЦД — хронічне безперервно прогресуюче захворювання, і лікар разом із пацієнтом 50:50 повинні контролювати його перебіг. Необхідно своєчасно виявити захворювання, призначити антигіперглікемічну терапію, досягати цільових показників рівня глюкози в крові натще, глікозильованого гемоглобіну, постпрандіальної глікемії. Фокус терапії пацієнтів із АГ, ЦД, ХХН та тривожним розладом має бути спрямований на подовження їхнього життя, підвищення його якості та профілактику ускладнень. Таким пацієнтам необхідно обов’язково призначати антигіпертензивну терапію, статинотерапію. Не слід зупинятися на неефективних дозах, обов’язково доводячи дозу до терапевтично ефективної.
2. В умовах сьогодення тривога стосується великої кількості людей, і пацієнтів із хронічним стресом стає все більше. Сімейний лікар вже на першому візиті може допомогти знизити рівень тривоги у пацієнта. Рекомендовано використання скринінгових шкал (хоча би HADS), елементів психоосвіти, доступних психотехнік, надання роз’яснень щодо зміни способу життя. Пацієнта (і, за можливості, родичів) слід залучати до терапії: пацієнт повинен бути співучасником лікувального процесу. Пояснення пацієнтам слід робити простою мовою, схемами, малюнками, не вводити заборону і не лякати.
3. До таких пацієнтів необхідний командний підхід. Залучення вузьких спеціалістів і призначення обґрунтованого лікування дозволять подовшити життя пацієнтів, покращити його якість і знизити ризик розвитку ускладнень.
Список використаної літератури
- 1. Unger T., Borghi C., Charchar F. et al. (2020) 2020 International Society of Hypertension Global Hypertension Practice Guidelines. Hypertension, 75(6): 1334–1357. doi: 10.1161/HYPERTENSIONAHA.120.15026.
- 2. ESC Clinical Practice Guidelines (2019) 2019 Guidelines on Chronic Coronary Syndromes. http://www.escardio.org/Guidelines/Clinical-Practice-Guidelines/Chronic-Coronary-Syndromes.
- 3. Gulati M., Levy Ph.D., Mukherjee D. et al. (2021) 2021 AHA/ACC/ASE/CHEST/SAEM/SCCT/SCMR Guideline for the Evaluation and Diagnosis of Chest Pain: A Report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Circulation, 144(22). doi.org/10.1161/CIR.0000000000001029.
- 4. ESC Clinical Practice Guidelines (2021) 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. http://www.escardio.org/Guidelines/Clinical-Practice-Guidelines/Acute-and-Chronic-Heart-Failure.
- 5. Holmes T.H., Rahe R.H. (1967) The Social Readjustment Rating Scale. J. Psychosom. Res., 11(2): 213–218.
- 6. Mancia G., Parodi A., Merlino L., Corrao G. (2011) Heterogeneity in antihypertensive treatment discontinuation be-tween drugs belonging to the same class. J. Hypertens., 29(5): 1012–1018. doi: 10.1097/HJH.0b013e32834550d0.
- 7. Peters S., Trümmel M., Meyners W. et al. (2005) Valsartan versus ACE inhibition after bare metal stent implantation — results of the VALVACE trial. Int. J. Cardiol., 98(2): 331–335. doi: 10.1016/j.ijcard.2004.05.062.
- 8. Ko D., Azizi P., Koh M. et al. (2019) Comparative effectiveness of ACE inhibitors and angiotensin receptor blockers in patients with prior myocardial infarction. Open Heart, 6(1): e001010. doi: 10.1136/openhrt-2019-001010.
- 9. Elliott W.J., Meyer P.M. (2007) Incident diabetes in clinical trials of antihypertensive drugs: a network meta-analysis. Lancet, 369(9557): 201–207. doi: 10.1016/S0140-6736(07)60108-1.
- 10. Kennedy S.H., Lam R.W., McIntyre R.S.; CANMAT Depression Work Group (2016) Canadian Network for Mood and Anxiety Treatments (CANMAT) 2016 Clinical Guidelines for the Management of Adults with Major Depressive Disorder: Section 3. Pharmacological Treatments. The Canadian Journal of Psychiatry/La Revue Canadienne de Psy-chiatrie, 1–21 р.
- 11. American Diabetes Association (2022) Standards of Medical Care in Diabetes-2022 Abridged for Primary Care Provid-ers. Clin. Diabetes, 40(1): 10–38. doi: 10.2337/cd22-as01.
- 12. Charytan D.M., Solomon S.D., Ivanovich P. et al. (2019) Metformin use and cardiovascular events in patients with type 2 diabetes and chronic kidney disease. Diabetes Obes. Metab., 21(5): 1199–1208. doi: 10.1111/dom.13642.
- 13. Yasuda T., Endoh M., Suzuki D. et al.; KVT Study Group (2013) Effects of valsartan on progression of kidney disease in Japanese hypertensive patients with advanced, predialysis, chronic kidney disease: Kanagawa Valsartan Trial (KVT). Hypertens. Res., 36(3): 240–246. doi: 10.1038/hr.2012.183.
- 14. Heerspink H.J.L., Stefánsson B.V., Correa-Rotter R. et al.; DAPA-CKD Trial Committees and Investigators (2020) Dapagliflozin in Patients with Chronic Kidney Disease. N. Engl. J. Med., 383: 1436–1446. DOI: 10.1056/NEJMoa2024816.
*Реальний клінічний випадок з лікарської практики.
**Фото акторки театру, яка зображає пацієнтку.





