ВСТУП
Хвороби серцево-судинної системи займають одне з провідних місць серед причин втрати працездатності та смертності у світі. Особливе значення з-поміж хвороб серцево-судинної системи має проблема інфаркту міокарда (ІМ) та гострої серцевої недостатності (СН) як його ускладнення, що асоціюється із значно вищою летальністю та гіршим прогнозом у таких хворих (Colonna P., Iliceto S., 2000; Крыжановский В.А., 2001; Лутай М.И., 2001). Останні роки в Україні та за кордоном велику увагу приділяють вивченню механізмів розвитку гострої СН та ролі ранньої систолічної дисфункції лівого шлуночка (ЛШ) у її прогресуванні (Pfeffer M.A., 2000; Лутай М.И., 2001).
У попередніх дослідженнях було показано вплив на виникнення та важкість перебігу гострої лівошлуночкової недостатності (ГЛШН) таких факторів, як розмір ІМ, локалізація ураження, гостра дисфункція мітрального клапана, дискоординація перед- та післянавантаження серця, наявність і вираженість кардіосклерозу, що передував ІМ (Dujardin K.S. et al., 1997; Kramer C.M. et al., 1997; Bodi V. et al., 1999; Bolognese L., Cerisano G., 1999). Розроблено схеми прогнозування перебігу ІМ залежно від наявності й вираженості ГЛШН за класифікацією T. Killip та J. Kimball (1967). Але залишаються остаточно не з’ясованими фактори, які сприяють виникненню ранньої систолічної дисфункції ЛШ у хворих на ІМ з зубцем Q (Q-ІМ), та її вплив на перебіг госпітального періоду й виходи ІМ у сучасних умовах лікування з широким використанням методів із доведеною ефективністю (тромболітична терапія, перкутанна транслюмінальна коронароангіопластика, інгібітори ангіотензинперетворювального ферменту (АПФ), блокатори β-адренорецепторів та ін).
Метою роботи було визначення особливостей клінічного перебігу Q-ІМ та морфофункціонального стану міокарда у хворих з ранньою систолічною дисфункцією ЛШ і факторів ризику несприятливого наслідку.
ОБ’ЄКТ І МЕТОДИ ДОСЛІДЖЕННЯ
Ретроспективно проаналізовано історії хвороб 476 пацієнтів з ІМ із зубцем Q, проведено оцінку систолічної функції ЛШ за допомогою ехокардіографії (ехоКГ). Вони перебували на лікуванні в інфарктному відділенні Центральної міської клінічної лікарні Києва з 1 січня по 31 грудня 2002 р.
До стаціонару протягом 12 год госпіталізовано 276 (58%) хворих, від 12 до 24 год — 97 (20,4%), після 24 год — 103 (21,6%) пацієнти. Середній вік хворих становив 68,2±0,74 року, серед них було 258 (54,2%) чоловіків та 218 (45,8%) жінок. Із дослідження виключено хворих із супутнім первинним ураженням клапанів внаслідок набутих вад серця. У 235 (49,4%) хворих була уражена передня стінка, у 241 (50,6%) — задня стінка ЛШ. ІМ в анамнезі був у 110 (23,1%) хворих, супутній цукровий діабет (ЦД) — у 106 (22,3%) пацієнтів. На час госпіталізації ГЛШН II–III класу за T. Killip та J. Kimball (1967) діагностували у 136 (28,6%) хворих, кардіогенний шок — у 30 (6,3%).
Хворим проводили загальноприйняте лікування (Van de Werf F. et al., 2003; Нетяженко В.З., 2004), яке включало ацетилсаліцилову кислоту (160–325 мг/добу) у 427 (89,7%), гепарин — у 380 (79,8%), блокатори
β-адренорецепторів — у 348 (73,1%), нітрати внутрішньовенно крапельно — у 407 (85,5%), інгібітори АПФ — у 393 (82,6%) хворих. Тромболізис було проведено у 20 (4,2%), первинну перкутанну транслюмінальну коронароангіопластику — у 31 (6,5%) хворих.
Для лікування при ГЛШН ІІ класу додатково застосовували діуретики (фуросемід внутрішньовенно у дозі 40–80 мг) і безперервну цілодобову інфузію нітрогліцерину, у разі ГЛШН ІІІ класу — додатково допамін у діуретичних дозах, при недостатній ефективності — також добутамін у стандартній дозі, при ГЛШН IV класу — додатково допамін у середніх та великих дозах. При порушеннях ритму враховували їхній характер та складність і використовували блокатори β-адренорецепторів, аміодарон, лідокаїн у загальноприйнятих дозах. При розвитку больового синдрому призначали наркотичні та ненаркотичні анальгетики і нейролептики.
Обстеження хворих, крім стандартного, включало ультразвукове дослідження серця у перші 3 доби захворювання на апараті «Philips SD800» — з визначенням параметрів систолічної та діастолічної функцій ЛШ за загальноприйнятою методикою (Feigenbaum H., 1990). Експансію зони гострого ІМ визначали за даними ехоКГ в дво- та чотирикамерній проекціях. Відповідно до рекомендації G.A. Lamas та співавторів (1989) критеріями експансії вважали витончення і деформацію контуру ЛШ зони інфарціювання. За модифікованим алгоритмом Сімпсона з перерахунком на одиницю площі поверхні тіла визначали кінцево-діастолічний (КДІ) і кінцево-систолічний (КСІ) індекси. Нормативні величини досліджуваних показників отримано при обстеженні 30 практично здорових осіб, зіставних за віком та статтю.
Статистичний аналіз результатів дослідження виконували на IBM PC/AT з використанням Excel 2002 та пакета статистичного аналізу SPSS 12.0. Для оцінки статистичної значущості відмінностей між групами порівняння використовували t-критерій.
РЕЗУЛЬТАТИ ТА ЇХ ОБГОВОРЕННЯ
Залежно від величини фракції викиду (ФВ) ЛШ, що була оцінена у перші 3 доби від моменту госпіталізації, хворих на Q-ІМ було розподілено на 2 групи: у 1-шу ввійшли пацієнти з систолічною дисфункцією міокарда ЛШ (ФВ<45%), у 2-гу — пацієнти зі збереженою систолічною функцією (ФВ≥45%). 1-шу групу становили 218 хворих (45,8%), 2-гу — 258 (54,2%), середній вік яких — 68,4±0,74 та 67,9±0,71 (р>0,05) року відповідно (табл. 1). Пацієнти з наявністю та без систолічної дисфункції ЛШ статистично значущо не відрізнялися також за статтю, частотою супутніх артеріальної гіпертензії (АГ), ЦД і тютюнопаління (р>0,05 в усіх випадках).
Слід зазначити, що в анамнезі у хворих із систолічною дисфункцією ЛШ значно частіше, ніж без неї, був ІМ — відповідно у 66 (30,3%) та 44 (17,1%) пацієнтів (р<0,01), в тому числі ІМ із зубцем Q — у 23 (10,6%) та 12 (4,7%) пацієнтів (р<0,01) (див. табл. 1).
Статистично значущу різницю між групами виявлено за кількістю пацієнтів, у яких ІМ передувала нестабільна стенокардія тривалістю понад 48 год. Так, у 1-й групі був 61 (28%) такий пацієнт, а в 2-й — 128 (49,6%) (р<0,001). Отже, можна припустити, що попередня нестабільна стенокардія асоціюється із нижчою частотою виникнення систолічної дисфункції ЛШ. Цей факт виявлено нами вперше, хоча у літературі є посилання на захисний ефект передінфарктної нестабільної стенокардії за рахунок реалізації феномену ішемічного прекондиціювання стосовно госпітальної летальності, частоти кардіогенного шоку та обширності ІМ (Bolognese L., Cerisano G., 1999; Крыжановский В.А., 2001; Пархоменко А.Н. и соавт., 2001).
У пацієнтів 1-ї групи частіше, ніж у таких 2-ї (р<0,001), була передня локалізація ІМ (62,4 проти 38,4%, р<0,001), тоді як у 2-й групі переважала задня локалізація ІМ (у 61,6 проти 37,6%, р<0,001). Щодо впливу систолічної дисфункції ЛШ на клінічний перебіг ІМ, то у пацієнтів з фракцією викиду <45% виявили значно більшу, ніж у хворих зі збереженою ФВ, частоту ГЛШН II–ІІІ класу (в 2,1 раза, р<0,001) та кардіогенного шоку (8,7 проти 0%), а також таких ускладнень, як рецидив ІМ (у 1,8 раза, р<0,05), госпітальна пневмонія (у 1,5 раза, р<0,01) (табл. 2). Більша частота блокади лівої (ЛНПГ — у 3,3 раза) та правої (ПНПГ) ніжки пучка Гіса (у 1,9 раза) (р<0,05 в обох випадках), імовірно, пов’язана з більшою кількістю хворих з переднім ІМ.
Привертає увагу той факт, що госпітальна летальність у хворих з ФВ<45% становила 42,5% і була в 4,5 раза вищою, ніж у пацієнтів з ФВ≥45% (р<0,01); серед причин смерті частота розриву міокарда становила 15,1 та 16,7% випадків у 1-й та 2-й групах відповідно (р>0,05).
Дані аналізу показників морфофункціонального стану серця та кардіогемодинаміки, за результатами ехоКГ, перших 3 днів госпіталізації у хворих на первинний Q-ІМ (1-ша група — 154 особи, 2-га — 215 осіб) наведено у табл. 3.
Зниження ФВ у хворих 1-ї групи (на 38,7%, р<0,001) відбувалося переважно за рахунок збільшення КСІ (на 87,5% порівняно з нормальними значеннями, р<0,001), а не КДІ (на 16,1%, р<0,01), що можна розцінити як встановлення неефективності закону Франка — Старлінга внаслідок вичерпання компенсаторно-пристосувальних реакцій неураженого міокарда, що загалом збігається з точкою зору інших дослідників (Bassand J.P., 1995; Лутай М.И., 2001; Пархоменко А.Н. и соавт., 2001).
Як видно з даних табл. 3, у хворих зі зниженою систолічною функцією ЛШ статистично значущо більшим, порівняно з нормою, був розмір ЛП (на 21,7%, р<0,01), ПШ (на 21,6%, р<0,05), НПВ (на 25,3%, р<0,05).
У середньому по 1-й групі відхилень від норми товщини ЗС ЛШ та МШП не було виявлено, проте при індивідуальному аналізі встановлено гіпертрофію ЛШ у 29,2% пацієнтів цієї групи.
У пацієнтів 2-ї групи зі збереженою насосною функцією ЛШ відхилення показників кардіогемодинаміки від відповідних значень у групі контролю були менш суттєвими, ніж у хворих 1-ї групи. ФВ була знижена на 11,5% (р<0,05) за рахунок збільшення КСІ на 18,7% (р<0,05) при незміненому КДІ, розмір ЛП перевищував аналогічний показник групи контролю на 17,6% (р<0,01), дилатація ПШ та НПВ була відсутня (р>0,05). Збільшувалась середня величина товщини ЗС та МШП (р<0,01) і гіпертрофія міокарда ЛШ у 57,7% хворих.
При порівнянні даних ехоКГ (див. табл. 3) виявлено статистично значущі відмінності між групами за всіма показниками, крім розмірів ЛП та ПШ.
Таким чином, для хворих з первинним Q-ІМ із систолічною дисфункцією ЛШ, на відміну від хворих із збереженою систолічною функцією, характерне ексцентричне ремоделювання ЛШ, що проявляється збільшенням КДІ ЛШ на 16,1% при незмінній товщині ЗС і МШП, потовщення яких порівняно із нормою на 33,3%, (р<0,05) характерне для хворих з ФВ≥45%. Систолічна дисфункція ЛШ супроводжувалась частішим, ніж при її відсутності, розвитком легеневої гіпертензії (р<0,01), а також дилатацією ПШ (на 21,6% порівняно зі здоровими особами, р<0,01) та НПВ (на 25,3%, р<0,05), що опосередковано свідчить про порушення систолічного спорожнення останнього.
Ексцентричне ремоделювання ЛШ у хворих 1-ї групи сприяло значно частішому, ніж при відносно збереженій систолічній функції ЛШ, розвитку феномену «expansion» (в 2,4 раза, а в підгрупі хворих з переднім ІМ — в 2,5 раза, р<0,001) і мітральної регургітації ішемічного ґенезу (в 3,2 раза, р<0,001).
При порівнянні хворих із систолічною дисфункцією ЛШ, що померли, та тих, що вижили, різниці між ними за віком, статтю, наявністю АГ не виявлено (р>0,05) (табл. 4).
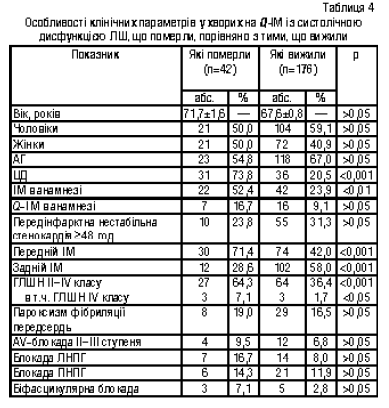
У хворих, котрі померли, значно частіше були ЦД, ІМ в анамнезі та передня локалізація ІМ (відповідно у 3,4; 2,2 та 1,7 раза, р<0,001); у хворих, що вижили, статистично значущо частіше, ніж у померлих (р<0,001), був ІМ задньої локалізації. За наявністю передінфарктної нестабільної стенокардії хворі статистично значущо не відрізнялись в обох групах (р>0,05), хоча в 2-й групі цей показник мав тенденцію бути більшим, і, можливо, за більшої вибірковості така різниця стала б статистично значущою.
У пацієнтів 1-ї групи значно частіше, ніж у хворих, котрі вижили, перебіг захворювання ускладнювався ГЛШН (р<0,001), в тому числі кардіогенним шоком (р<0,05), при чому це ускладнення, як правило, виникало після госпіталізації.
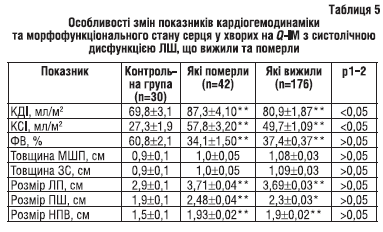
При аналізі параметрів внутрішньо-серцевої гемодинаміки у 1-шу—3-тю добу захворювання (табл. 5) виявлено, що у хворих, які померли, розміри КДІ та КСІ були більшими від показників у хворих, котрі вижили, відповідно на 7,9 і 16,3% (р<0,05 в обох випадках). У померлих хворих й тих, що вижили, суттєво не відрізнялись величини ПШ та ЛП (р>0,05).
ВИСНОВКИ
1. Факторами ризику розвитку ранньої систолічної дисфункції ЛШ при Q-ІМ є перенесений раніше ІМ та передня локалізація ІМ. Передінфарктна нестабільна стенокардія давністю понад 48 год асоціюється з меншим ризиком ранньої систолічної дисфункції ЛШ.
2. У хворих з Q-ІМ у сучасних умовах його лікування рання систолічна дисфункція ЛШ асоціюється з підвищенням госпітальної летальності в 4,5 раза внаслідок підвищення частоти ГЛШН в 2,1 раза, а також кардіогенного шоку і супроводжується підвищенням частоти рецидиву ІМ в 1,8 раза.
3. Хворі первинним Q-ІМ з ранньою систолічною дисфункцією ЛШ відрізнялися від хворих без неї розвитком раннього ексцентричного ремоделювання ЛШ, якому сприяла більша частота «expansion» зони інфарціювання та ішемічної мітральної регургітації, а також дилатацією ПШ та НПВ.
4. У хворих з Q-ІМ та ранньою систолічною дисфункцією ЛШ несприятливе прогностичне значення мають ЦД та ІМ в анамнезі, передня локалізація ІМ, ГЛШН при госпіталізації. Несприятливий прогноз асоціюється з більш вираженою ранньою дилатацією порожнини ЛШ в кінці діастоли та систоли.
ЛІТЕРАТУРА
- Крыжановский В.А. (2001) Диагностика и лечение инфаркта миокарда. Феникс, Киев, 451 с.
- Лутай М.И. (2001) Систолическая дисфункция левого желудочка у больных с ишемической болезнью сердца. Клиническое значение гибернированного миокарда. Doctor, 4: 30–34.
- Нетяженко В.З. (2004) Особливості ведення окремих категорій хворих із гострим інфарктом міокарда і елевацією сегмента ST та стратифікація ризику (за рекомендаціями Європейського товариства, 2002). Ліки України, 1: 10–14.
- Пархоменко А.Н., Иркин О., Кушнир С. (2001) Клинические аспекты постинфарктного моделирования левого желудочка сердца: от поражения миокарда к сердечной недостаточности. Doctor, 4: 36–39.
- Bassand J.P. (1995) Left ventricular remodelling after acute myocardial infarction — solved and unsolved issues. Eur. Heart J., 16(Suppl. I): 58–63.
- Bodi V., Sanchis J., Berenguer A., Insa L.D., Chorro F.J., Llacer A., Lopez-Merino V. (1999) Wall motion of noninfarcted myocardium. Relationship to regional and global systolic function and to early and late left ventricular dilation. Int. J. Cardiol., 71(2): 157–165.
- Bolognese L., Cerisano G. (1999) Early predictors of left ventricular remodeling after acute myocardial infarction. Am. Heart J., 138(2 Pt 2): S79–83.
- Colonna P., Iliceto S. (2000) Myocardial infarction and left ventricular remodeling: results of the CEDIM trial. Carnitine Ecocardiografia Digitalizzata Infarto Miocardico. Am. Heart J., 139(2 Pt 3): S124–130.
- Dujardin K.S., Enriquez-Sarano M., Rossi A., Bailey K.R., Seward J.B. (1997) Echocardiographic assessment of left ventricular remodeling: are left ventricular diameters suitable tools? J. Am. Coll. Cardiol., 30(6): 1534–1541.
- Feigenbaum H. (1990) Role of echocardiography in acute myocardial infarction. Am. J. Cardiol., 66(18): 17H–22H.
- Killip T. 3rd, Kimball J.T. (1967) Treatment of myocardial infarction in a coronary care unit. A two year experience with 250 patients. Am. J. Cardiol., 20(4): 457–464.
- Kramer C.M., Rogers W.J., Theobald T.M., Power T.P., Geskin G., Reichek N. (1997) Dissociation between changes in intramyocardial function and left ventricular volumes in the eight weeks after first anterior myocardial infarction. J. Am. Coll. Cardiol., 30(7): 1625–1632.
- Lamas G.A., Vaughan D.E., Parisi A.F., Pfeffer M.A. (1989) Effects of left ventricular shape and captopril therapy on exercise capacity after anterior wall acute myocardial infarction. Am. J. Cardiol., 63(17) 1167–1173.
- Pfeffer M.A. (2000) Enhancing cardiac protection after myocardial infarction: rationale for newer clinical trials of angiotensin receptor blockers.Am. Heart J., 139(1 Pt 2): S23–28.
- Van de Werf F., Ardissino D., Betriu A., Cokkinos D.V., Falk E., Fox K.A., Julian D., Lengyel M., Neumann F.J., Ruzyllo W., Thygesen C., Underwood S.R., Vahanian A., Verheugt F.W., Wijns W.; Task Force on the Management of Acute Myocardial Infarction of the European Society of Cardiology (2003) Management of acute myocardial infarction in patients presenting with ST-segment elevation. The Task Force on the Management of Acute Myocardial Infarction of the European Society of Cardiology. Eur. Heart J., 24(1): 28–66.
Резюме. Проведен анализ особенностей клинического течения и морфофункционального состояния миокарда у больных с Q-инфарктом миокарда с ранней систолической дисфункцией левого желудочка, изучены факторы, обусловливающие ее развитие, и факторы риска неблагоприятного исхода у таких больных.
Ключевые слова: инфаркт миокарда, систолическая дисфункция левого желудочка, прогноз
Summary. Features of clinical course and morphofunctional state of myocardium in patients with Q-myocardial infarction and early left ventricular systolic dysfunction were studied. Predictors of early left ventricular systolic dysfunction in patients with Q-wave myocardial infarction and factors of unfavorable outcome are presented.
Key words: myocardial infarction, left ventricular systolic dysfunction, prognosis





