ВСТУП
Відомо, що стовбурові інсульти — найчастіша причина розвитку нейрогенної ротоглоткової дисфункції. Часто ознаки нейрогенної дисфагії поєднані з іншими симптомами бульбарного синдрому — дисфонією та дизартрією. Вартим уваги є повідомлення, що гостра фарингеальна дисфагія може бути первинною маніфестацією інсульту в стовбурі головного мозку (Buchholz D.W., 1993).
Нейрогенна дисфагія після розвитку півкульного інсульту виникає за умови двобічного ураження кірково- ядерних шляхів, що зумовлює розвиток псевдобульбарного синдрому. Однобічні півкульні інсульти також викликають дисфагію, хоча не так часто як двобічні.
Патофізіологія нейрогенної ротоглоткової дисфагії є мультифакторіальною і пов’язана з розладами аферентних та еферентних функцій нервової системи і порушенням механізмів захисту повітроносних шляхів під час акту ковтання (Таbаеe A. et al., 2005, Віничук С.М., Волосовець А.О. 2008а).
Термін «дисфагія» слід використовувати у тому разі, коли виявляються відповідні симптоми, пов’язані з порушенням ковтання: затримка решток їжі в роті, недостатнє очищення ротової порожнини; утруднення проходження їжі в глотці, подовжений глотковий ковток; назальна регургітація; кашель або поперхнення при ковтанні та ознаки аспірації їжі при харчуванні; накопичення слини в роті; порушення мови (зміна голосу, «вологий» голос, невиразна, «булькаюча» мова); парез м’якого піднебіння тощо. До того ж виявлення певних вищезазначених симптомів без чіткого порушення функції ковтання не свідчить про наявність нейрогенної дисфагії в пацієнта.
Дисфагія в гострий період мозкового інсульту є несприятливою прогностичною ознакою, що призводить до таких ускладнень, як легенева аспірація і дегідратація, погіршення енергетичного обміну тощо. Їх можна уникнути в тому разі, якщо нейрогенна дисфагія буде своєчасно виявлена та пролікована. На жаль, лікарі часто не виявляють порушення ковтальної функції у пацієнтів.
Існують різні методи дослідження функції ковтання. Оцінка їх позитивних та негативних характеристик має важливе значення для оптимального ведення хворого з дисфагією.
Методи діагностики нейрогенної дисфагії
Клінічні методи. Для оцінки порушень функції ковтання у пацієнта після перенесеного гострого мозкового інсульту, безумовно, перевага надається клінічним методам обстеження безпосередньо біля ліжка хворого. Оскільки достеменно не встановлено, який з методів точніше визначає клінічно несприятливі ознаки дисфагії, рекомендують скринінговий підхід виявлення порушення ковтальної функції (Ворлоу Ч.П. та співавт., 1998). Зокрема, з урахуванням даних неврологічного дефіциту виділяють хворих з ризиком виникнення порушень ковтання: тяжкий стовбуровий або півкульний інсульт з порушенням свідомості; пацієнти з афазією, геміанопсією, автотопагнозією; вираженим парезом мімічних м’язів; наявність або відсутність кашлю або зміни в голосі («вологий» голос або «булькаюча» мова); зниження чутливості глотки; наявність парезу м’якого піднебіння; дані про інфекційний процес у легенях.
Доцільно оцінювати функцію ковтання за допомогою тесту «пробного ковтання»: пацієнта підтримують у сидячому положенні й просять проковтнути 50 мл води, починаючи з 5 мл. Об’єм та швидкість спожитої рідини контролюють за допомогою питної трубочки: мимовільний кашель або зміни в голосі пацієнта можуть свідчити про легеневу аспірацію. Виявлення її важливе, оскільки безсимптомна аспірація є несприятливим чинником ризику розвитку бронхопневмонії (Holas M.A. et al., 1994). Поперхнення — очевидна ознака дисфагії. У цьому разі можуть також спостерігатись дисфонія, дизартрія, порушення ритму дихання (диспное).
Інколи деякі хворі в разі споживання їжі намагаються компенсувати порушення ковтання за допомогою частого вживання рідини під час їди для переміщення харчового болюсу в стравохід. При огляді ротової порожнини у них можна знайти залишки їжі та надлишок слини, які накопичуються в глотці та розповсюджуються за голосові зв’язки в трахею.
Вимірювання швидкості ковтання в пацієнта — невід’ємна складова клінічних методів діагностики нейрогенної дисфагії. Хворому в положенні сидячи пропонують проковтнути 150 мл прохолодної води та вимірюють швидкість глоткового транзиту. У разі неможливості прийняття рідини безпосередньо з посуду пацієнту пропонують аспірувати її крізь пластикову трубочку. Про наявність дисфагії свідчить швидкість ковтання <10 мл/с. Можливі наявні прояви дисфагії: подовжені часові проміжки між ковтками, виливання води з ротової порожнини, вологий кашель. Цей тест достатньо чутливий і достовірний (Nathadwarawala K.M. et al., 1992), але не дає повного уявлення про ступінь вираженості нейрогенної дисфагії. Крім того, недоліком методу є неможливість виконання його у хворих з тяжким і надто тяжким інсультом.
Ненадійним показником можливого порушення ковтання у пацієнтів, які перенесли мозковий інсульт, є ослаблення або відсутність глоткового рефлексу (Smithard D.G., 1998). За даними Daniels A.E. та співавторів (1997), майже у 30% здорових людей молодого та у 47% людей старшого віку можлива одно- чи двобічна відсутність глоткового рефлексу.
Радіологічні методи. Відеофлюороскопія (ВФ) (або тест з ковтанням барію) часто розглядається як «золотий стандарт» оцінки функції ковтання (Horner J., Massey E.W., 1998; O’Donoghue S., Bagnall A., 1999). Вона дозволяє спостерігати за підготовчою ротовою фазою ковтання, ініціацією ковтального рефлексу та за глотковим транзитом болюсу (Bakheit A.M., 2001). Методика відеофлюороскопії проводиться наступним чином: пацієнт сидить під кутом від 45 до 90° та поглинає рідину або їжу різної консистенції, імпрегновану барієм. Процес ковтання візуалізується в латеральній та передньозадній проекціях. ВФ дає змогу здійснювати динамічне дослідження ковтального процесу, дозволяє радіологу обстежити анатомічні структури, функціональний стан оральної та фарингеальної фаз ковтання, оцінити ефективність застосованих реабілітаційних заходів.
З існуючих методів оцінки функції ковтання ВФ дозволяє точніше визначити клінічно важливі складові дисфагії, тобто ті, які призводять до можливих ускладнень. Методика достатньо чутлива, а її результати корелюють з іншими застосованими методами обстеження (Scott A. et al., 1998). Зокрема, збіг діагнозів логопеда та радіолога становить r=0,75±0,09 (Mann G. et al., 2000).
Хоча відеофлюороскопія і вважається золотим стандартом діагностики дисфагії, використання її для обстеження хворих з гострим інсультом безпосередньо біля ліжка є обмеженим: за умови необхідності постійного моніторингу функції ковтання; небажання пацієнтів проводити дослідження через додаткове іонізуюче випромінення чи брак коштів; наявний ризик ураження легень у разі аспірації радіоконтрасту тощо. До того ж проведення ВФ у клініці та оцінка отриманих результатів потребує спеціального обладнання та підготовленого персоналу (DePippo K.L. et al., 1992; Stanners A.J., et al., 1993).
Латеральна шийна м’якотканинна радіографія також проводиться за умови застосування спеціального контрасту. Водночас оцінка отриманих результатів часто складна і залежить навіть від зміни положення голови пацієнта. Безумовно, це знецінює загальну значимість дослідження (Bakheit A.M., 2001).
Ізотопна сцинтіграфія також не має переваг перед іншими індикаторними методами. До того ж це інвазивний метод дослідження, який потребує спеціального обладнання та підготовки відповідного персоналу (Muz J. et al., 1991).
Електрофізіологічні методи. Електроміографію (ЕМГ) здебільшого використовують для оцінки функціонального стану м’язового ковтального апарату у пацієнтів з міастенією (Ertekin С. et al., 1998). Однак її використовують як допоміжну методику також для оцінки функції ковтання у пацієнтів у гострий період мозкового інсульту (Ertekin С. et al., 1995). За допомогою полярних відведень механічного сенсору реєструють глоткові рухи вверх і вниз. Сенсор відповідним чином з’єднаний з апаратом ЕМГ. Використання цієї методики дозволяє встановити «дисфагічний поріг» для сухого та вологого типів ковтання. Цей тест полягає у визначенні кількості води (від 1 до 20 мл), яку пацієнт не розділяючи може проковтнути одним ковтком (Lоgeman J.A., 1983). Здебільшого поріг дисфагії не вищий 20 мл. У разі значної ротоглоткової дисфункції поріг дисфагії <1 мл, а ковтання супроводжується кашлем, що свідчить про легеневу аспірацію. Методика інвазивна і досить складна для здійснення біля ліжка пацієнта, який переніс інсульт.
Досліджененя газів крові. Пульсова оксиметрія — це методика оцінки ступеня порушення акту ковтання, яка грунтується на припущенні, що аспірація рідини чи їжі в повітроносні шляхи викликає рефлекторний бронхоспазм. Останній в свою чергу призводить до порушення вентиляційно- перфузійного співвідношення в легенях. Відомо, що для адекватного газообміну в легенях необхідно, щоб вентиляція відповідала перфузії, тобто щоб були адекватними вентиляційно-перфузійні співвідношення в легенях (Zaidi N.Н. et al., 1995). У разі дисфагії аспірація спричиняє рефлекторний бронхоспазм і призводить до вентиляційно- перфузійного дисбалансу: неоксигенована і не позбавлена СО2 кров поступає в артеріальне русло великого кола кровообігу, що призводить до гіпоксемії та гіперкапнії. Тому досить часто у пацієнтів після ковтання води в гострий період мозкового інсульту виявляється значна десатурація (Zaidi N.Н. et al., 1995).
Дефіцит насичення киснем артеріальної крові вимірюється саме за допомогою методу пульсової оксиметрії. Вважають, що ця методика може свідчити про наявність аспірації у 81,5% випадків нейрогенної дисфагії після перенесеного інсульту. Показник чутливості коливається від 77,0 до 87,0% (Collins M.J. et al., 1997). Метод неінвазивний і може використовуватися для моніторингу за станом пацієнта. Водночас отримані результати необхідно оцінювати, враховуючи факт тютюнопаління хворим і наявність хронічних захворювань легень у пацієнта, оскільки висока концентрація карбоксигемоглобіну в крові може давати хибні або негативні результати.
Отже, пульсова оксиметрія — корисна методика для виявлення кисневої десатурації, яка може бути ознакою аспірації, що часто супроводжує дисфагію в разі мозкового інсульту. Однак отримані результати дослідження повністю не відображають прояви дисфагії, а відіграють лише допоміжну роль у діагностиці проявів легеневої аспірації.
Інші додаткові методи. Фіброоптична ендоскопія передбачає введення ендоскопічної трубки в носову порожнину та фіксування її над м’яким піднебінням. Потім пацієнту пропонують ковтати відповідним чином забарвлену їжу і спостерігають за актом ковтання. Фіброоптична ендоскопічна оцінка функції ковтання дозволяє отримати інформацію про анатомічні структури, функціонування ковтального рефлексу, глоткову рухову стадію ковтання, виявляє чутливі порушення глотки. Безпосередньо за допомогою цієї методики візуалізувати аспірацію неможливо, але про її наявність можуть свідчити виявлені залишки їжі в ротовій порожнині після ковтання або викид діагностичного матеріалу з трахеї через кашель (Zaidi N.Н. et al., 1995; Aviv J.E. et al., 1998).
Дослідження безпечне, може бути проведене біля ліжка хворого, нормально сприймається хворими (Aviv J.E. et al., 2000). Можливе здійснення відеозображення. Але виконання процедури залежить від кваліфікації лікаря та якісного обладнання. Крім того, це дослідження надає недостатню інформацію про оральну та стравохідну стадії акту ковтання (Ramsey D.J. et al., 2003).
Цервікальна аускультація механічного чи/та респіраторного компоненту акту ковтання також дає певну інформацію. Порівняння ступеня вираженості дисфагії за цією методикою з ВФ виявило вірогідний збіг діагностованої легеневої аспірації (Zenner P.M. et al., 1995). Обстеження можна провести безпосередньо біля ліжка хворого, але досі не встановлені чіткі аускультативні звукові еталони і техніка проведення цервікальної аускультації.
Ультрасонографія є безпечним та порівняно мобільним методом дослідження, але більшість ультразвукових датчиків замалі для того, щоб візуалізувати весь процес акту ковтання. До того ж ділянка обстеження (шия) обмежена безкістковими ділянками (Smithard D.G. et al., 2002).
Фарингеальна або езофагеальна манометрія може надати корисну інформацію, особливо коли проводиться в комбінації з ВФ (Hila A. et al., 2001). Це дослідження дозволяє вимірювати градієнт внутрішньостравохідного тиску та оцінити порушення функції крікофарингеального м’яза, розслаблення якого започатковує перехід до подальшої стравохідної стадії акту ковтання.
Таким чином, аналіз клінічних методів оцінки нейрогенної дисфагії у хворих, які перенесли мозковий інсульт, свідчить про їх безпеку та можливість широко використовувати безпосередньо біля ліжка хворого. Щоправда, чутливість та специфічність клінічних тестів різна, і не завжди вони дозволяють виявляти наявність прихованої аспірації. Крім того, існуючі клінічні методи не дають повного уявлення про ступінь вираженості нейрогенної дисфагії. Дослідження функції ковтання з використанням радіологічних, електрофізіологічних методик мають свої переваги та недоліки порівняно з клінічними тестами, але їх впровадження обмежене, оскільки потребує відповідного обладнання та спеціалізованого персоналу для його обслуговування і ведення хворих з нейрогенною дисфагією. Пульсову оксиметрію доцільно використовувати в комплексі з клінічними методами оцінки функції ковтання. Цінну інформацію про нейрогенну ротоглоткову дисфункцію в гострий період мозкового інсульту надає фіброоптична ендоскопія, але проведення її дослідження також потребує відповідного обладнання і підготовленого персоналу. Значущість інших методів діагностики функції ковтання (цервікальна аускультація, ультрасонографія, фарингеальна чи езофагеальна манометрія) невисока в оцінці ковтальної механіки.
Суттєві обмеження та недостатня інформативність більшості застосованих методів діагностики ротоглоткової дисфункції та оцінки порушень ковтання диктують необхідність розробки й впровадження об’ єктивніших і простих у використанні критеріїв оцінки порушень ковтальної функції в пацієнтів з нейрогенною дисфагією в гострий період мозкового інсульту.
Звичайно, для лікаря-невролога критеріями діагностики дисфагії були і залишаються дані неврологічного та соматичного обстеження. Правильна їх оцінка значною мірою залежить від досвіду лікаря. На жаль, і за таких умов неможлива об’єктивна оцінка вираженості дисфагічних порушень в гострий період мозкового інсульту.
Тепер у різних галузях медицини існує багато розроблених за певними аспектами формалізованих систем діагностики різних видів патології, окремих клінічних проявів. Найоптимальнішими для використання є методологія ймовірнісного аналізу Байєса і методика неоднорідної послідовної статистичної процедури Вальда — Генкіна — Гублера (Генкін А.А., Гублер Е.В., 1964).
На нашу думку, наявність в арсеналі лікаря-невролога бальної оцінки вираженості нейрогенної дисфагії з використанням клінічних неврологічних шкал суттєво допомогла б поліпшити якість діагностики ротоглоткової дисфункції та патронування таких хворих у гострий період мозкового інсульту.
Мета дослідження — розробити неврологічну шкалу оцінки ротоглоткової дисфункції в пацієнтів з нейрогенною дисфагією в гострий період мозкового інсульту, використовуючи клінічні критерії, пов’язані з порушенням функції ковтання, а також методологію ймовірнісного аналізу Байєса й алгоритм послідовної статистичної процедури Вальда — Генкіна — Гублера.
ОБ’ЄКТ І МЕТОДИ ДОСЛІДЖЕННЯ
База даних для побудови неврологічної шкали та створення системи клінічної діагностики нейрогенної дисфагії та оцінки її вираженості в балах ґрунтувалась на обстеженні 108 пацієнтів з гострим мозковим інсультом (67 чоловіків та 41 жінка) віком від 32 до 88 років (середній вік — 63,3±1,12 року). Діагноз «мозковий інсульт» встановлювали за даними клініко- неврологічного обстеження, а також спіральної комп’ютерної томографії (СКТ) та магнітно- резонансної томографії (МРТ). Залежно від наявності в неврологічному статусі нейрогенної дисфагії хворих розподілили на дві групи.
До 1-ї (група А1) увійшли 65 пацієнтів віком від 32 до 88 років (середній вік — 63,9±1,47 року), у яких неврологічні розлади поєднувалися із нейрогенною дисфагією різного ступеня вираженості. У 55 хворих дисфагія виникла після ішемічного інсульту, а у 10 — зумовлена гострим розвитком внутрішньомозкового крововиливу. У 47 обстежених порушення мозкового кровообігу виникло в судинах вертебрально- базилярного басейну (ВББ), ще в 18 — у каротидному (правопівкульна — у 6, лівопівкульна — у 3, двопівкульна — у 9).
До 2-ї групи (А2) були залучені 43 пацієнти віком від 46 до 76 років (середній вік — 62,6±1,1 року) без ознак порушення ковтання. Півкульні інфаркти виявили у 34 пацієнтів, стовбурові — у 9. Отже, досліджувані групи були зіставні за віком і мали аналогічну локалізацію вогнища ураження.
Для побудови шкали оцінки функції ковтання у пацієнтів, які перенесли гострий мозковий інсульт, була розроблена формалізована історія хвороби, в якій детально аналізувалися понад 30 клінічних симптомів. Вони відображали об’єм неврологічного дефіциту за шкалою NIHSS (National Institutes of Health Stroke Scale/шкала інсульту Національних інститутів здоров’ я) і додатково детально характеризували ротоглоткову дисфункцію. Клінічні критерії підрозділяли на декілька градацій, відповідно до їх вираженості. Спочатку складали таблицю частоти симптомів із зазначенням ступеня їх вираженості (табл. 1). Для цього визначали, яка кількість хворих (Аij) мала j-градацію вираженості і- симптому (Sij), розраховували їх частоту у відсотках РА(Sij) серед загальної кількості обстежених (NiA):
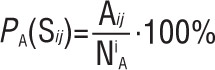
Таблиця 1
Клінічні ознаки та їх частота у хворих з гострим мозковим інсультом і проявами дисфагії та без такої (%)
|
Клінічні ознаки |
Група пацієнтів |
|
|
А1 (n=65) |
А2 (n=43) |
|
|
Важкість ініціації акту ковтання |
100 |
15 |
|
Затримка глоткового транзиту |
100 |
0 |
|
Кашель та ознаки аспірації під час ковтання |
100 |
11 |
|
Слабкість мімічних м’язів |
100 |
100 |
|
Дисфонічна «булькаюча» мова |
86 |
11 |
|
Затримка їжі в ротовій порожнині |
75 |
5 |
|
Накопичення слини в роті (порушення управління слиновиділенням) |
71 |
5 |
|
Знижений глотковий рефлекс |
69 |
35 |
|
Назальна регургітація |
65 |
5 |
|
Дизартрія |
65 |
58 |
|
Парез м’якого піднебіння |
54 |
39 |
|
Ненормальна поза при ковтанні |
46 |
23 |
|
Повільне підняття глотки |
40 |
13 |
|
Втрата маси тіла |
37 |
18 |
|
Легенева інфекція |
18 |
10 |
|
Відчуття комку за грудиною |
12 |
9 |
|
Слабкість м’язів язика |
12 |
11 |
|
Слабкість жувальних м’язів |
7 |
11 |
Клінічні ознаки, виявлені у хворих з нейрогенною дисфагією після мозкового інсульту, були порівняні з аналогічними розладами пацієнтів без ротоглоткової дисфункції. Слід зазначити, що цінність частоти виявлення окремих клінічних показників була недостатньо інформативною. Тому перший етап побудови неврологічної шкали для оцінки функції ковтання у хворих передбачав визначення для кожної ознаки діагностичного коефіцієнту (ДК). Це величина, яка відображає кількісну оцінку впливу клінічної ознаки на формування нейрогенної ротоглоткової дисфагії в обстежених групах А1 і А2. Розрахунки здійснювали з урахуванням імовірнісного аналізу Байєса за методикою неоднорідної послідовної процедури (Генкін А.А., Гублер Е.В., 1964), яка ґрунтується на послідовному статистичному аналізі А. Вальда:
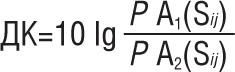
Визначали також ДК для кожної градації кожного симптому. Потім порівнювали величини ДК окремих клінічних ознак пацієнтів досліджуваних груп і розташовували у таблиці в порядку зменшення їх інформативної цінності. За допомогою критерію χ² Пірсона визначили клінічні симптоми, за якими пацієнти груп А1 та А2 статистично значимо відрізнялися. Виявилось, що високу ймовірність на формування нейрогенної дисфагії після мозкового інсульту мали 7 клінічних ознак (табл. 2).
Таблиця 2
Інформативність клінічних ознак ризику розвитку нейрогенної дисфагії в гострий період мозкового інсульту
|
Клінічні ознаки |
ДК |
p |
|
1. Затримка глоткового транзиту |
21,7 |
<0,001 |
|
2. Затримка їжі в ротовій порожнині |
13,5 |
<0,002 |
|
3. Порушення управління слиновиділенням |
13,2 |
<0,01 |
|
4. Назальна регургітація |
12,9 |
<0,01 |
|
5. Кашель і ознаки аспірації під час ковтання |
12,2 |
<0,01 |
|
6. Дисфонічна «булькаюча» мова |
10,6 |
<0,05 |
|
7. Важкість ініціації акту ковтання |
10,0 |
<0,05 |
Кожен із наведених параметрів мав високий рівень інформативності щодо формування нейрогенної дисфункції в гострий період мозкового інсульту. Інформативність розраховували з урахуванням діагностичних коефіцієнтів кожної з клінічних ознак. Для побудови діагностичної шкали не використовували клінічні ознаки з низьким рівнем інформативності.
Ця статистично узагальнена симптоматика слугувала еталоном, з яким порівнювали ступінь подібності виявлених у пацієнтів з нейрогенною дисфагією симптомів. До того ж інформативність окремих клінічних ознак не була вирішальною, а їх діагностична цінність підвищувалась лише у взаємозв’язку з іншими клінічними показниками. Наведені клінічні ознаки відповідно до їх ступеня тяжкості підрозділяли на декілька градацій. Для кожної j-градації кожного симптому визначали діагностичні коефіцієнти, які для зручності розрахунку округляли до одиниці й оцінювали в балах. Максимальна вираженість патологічної ознаки відповідала оцінці в 1 бал, а мінімальні прояви або нормальна функціональність ознаки — 5 балів.
Згідно з результатами, отриманими на підставі алгоритму послідовної статистичної процедури, була побудована неврологічна шкала бальної оцінки нейрогенної дисфагії в гострий період мозкового інсульту (Віничук С.М., Волосовець А.О., 2008б). Вона передбачає обстеження хворого з урахуванням 7 вищезазначених клінічних проявів, пов’язаних з порушенням функції ковтання. Звичайно, важливе значення мало визначення j-градації кожного симптому та правильна оцінка його в балах. Максимальна кількість балів за розробленою шкалою 35, мінімальна — 7.
Нейрогенну дисфагію в гострий період мозкового інсульту оцінюють таким чином. Спочатку використовують тест вимірювання швидкості ковтання (хворому пропонують ковтнути 150 мл прохолодної води); швидкість глоткового транзиту <10 мл/с свідчить про наявність дисфагії.
Для визначення ступеня вираженості нейрогенної дисфагії в гострий період мозкового інсульту застосовують шкалу оцінки ротоглоткової дисфункції за 7 клінічними проявами, що характеризують порушення функції ковтання (див. табл. 3).
Таблиця 3
Шкала оцінки тяжкості нейрогенної дисфагії
|
Клінічні ознаки |
Ступінь вираженості патологічної ознаки |
Бал |
|
1. Затримка глоткового транзиту Проводять ретельний аналіз зібраного харчового анамнезу, досліджують глотковий рефлекс та визначають консистенцію їжі, глотковий транзит якої порушено. Використовують тест вимірювання швидкості ковтання |
Їжа будь-якої консистенції вільно проходить через глотку в стравохід |
5 |
|
Спостерігається незначна затримка при проходженні їжі через глотку в стравохід |
4 |
|
|
Час проходження їжі через глотку дещо подовжений, спостерігаються додаткові допоміжні ковтальні рухи (швидкість ковтання <10 мл/с) |
3 |
|
|
Транзит харчового болюсу через глотку порушений, час проходження їжі значно подовжений |
2 |
|
|
Транзит їжі через глотку відсутній, пероральне харчування неможливе |
1 |
|
|
2. Затримка їжі в ротовій порожнині З’ясовують у хворого про можливі незручності в разі вживання їжі різної консистенції (виливання рідин з ротової порожнини, затримка залишків твердої їжі у щічних кишенях тощо), уважно оглядають ротову порожнину на наявність решток їжі, звертають увагу на прояви щічно-язикової апраксії |
Хворий вільно вживає їжу будь-якої консистенції, їжа не затримується в ротовій порожнині |
5 |
|
Наявна незначна затримка транзиту їжі в ротовій порожнині (переважно твердої консистенції) |
4 |
|
|
Спостерігається затримка харчового болюсу в ротовій порожнині при вживанні їжі твердої консистенції |
3 |
|
|
Наявні ознаки затримки рідкої та напіврідкої їжі в ротовій порожнині, транзит твердої їжі значно порушений |
2 |
|
|
Повністю порушений транзит твердої їжі та рідини через ротову порожнину, спожита вода виливається прямо з рота |
1 |
|
|
3. Порушення управління слиновиділенням Проводять обстеження ротової порожнини на наявність гіпер- або гіпосалівації, здійснюють спостереження за непрямими ознаками цих проявів (витікання слини з рота, патологічна сухість слизової оболонки ротової порожнини тощо) |
Контроль слиновиділення не порушений, слина вільно ковтається |
5 |
|
Спостерігаються незначні утруднення при відсмоктуванні та ковтанні слини |
4 |
|
|
Наявні помірні порушення при відсмоктуванні та ковтанні слини, з’являється відчуття «комка» у горлі |
3 |
|
|
Глибокі розлади управління слиновиділенням, відсмоктування та ковтання слини значно порушене |
2 |
|
|
Неможливість відсмоктування та ковтання слини, остання накопичується в ротовій порожнині і періодично стікає з кутів рота |
1 |
|
|
4. Назальна регургітація Обстеження включає детальне розпитування хворого про наявні випадки потрапляння їжі в носову порожнину, дослідження екскурсії та тонусу м’якого піднебіння та ідентифікація можливої носової регургітації при виконанні «ковтального» тесту |
Назальна регургітація відсутня, їжа не потрапляє в носоглотку |
5 |
|
Наявне незначне потрапляння води в носову порожнину при ковтанні |
4 |
|
|
Спостерігається помірне потрапляння елементів рідкої їжі та води в носову порожнину |
3 |
|
|
Значне потрапляння крихт твердої їжі та елементів рідкої їжі та води в носову порожнину внаслідок затримки транзиту харчового болюсу |
2 |
|
|
Постійне потрапляння елементів їжі будь-якої консистенції в носову порожнину внаслідок порушення транзиту харчового болюсу |
1 |
|
|
5. Кашель та ознаки легеневої аспірації Звертають увагу на кашель та вологі «булькаючі» хрипи, що можуть спостерігатись у хворого при проведенні «ковтального» тесту. Для виявлення легеневої аспірації чи розвитку аспіраційної пневмонії проводять аускультацію грудної порожнини |
Відсутність кашлю, поперхнення та інших ознак аспірації під час прийому їжі |
5 |
|
Спостерігається незначне відкашлювання в процесі харчування |
4 |
|
|
Наявні помірний кашель та поперхнення внаслідок порушення процесу закриття повітроносних шляхів при ковтанні |
3 |
|
|
Значні прояви аспірації, постійний кашель під час їди |
2 |
|
|
Прояви аспірації близькі до асфіксії, неможливість проведення повноцінного акту ковтання |
1 |
|
|
6. Дисфонічна «булькаюча» мова Для адекватної оцінки ступеня вираженості цієї ознаки хворому задають ряд запитань і оцінюють артикуляцію мови |
Порушення мови відсутні |
5 |
|
Спостерігаються незначні відхилення мовлення, мова пацієнта зрозуміла, але нечітка |
4 |
|
|
Помірні розлади мови, з’являються елементи «булькаючої» мови |
3 |
|
|
Значні розлади мовлення, пацієнта важко зрозуміти, дисфонічна «булькаюча» мова |
2 |
|
|
Мова пацієнта цілком незрозуміла |
1 |
|
|
7. Тяжкість ініціації акту ковтання Звертають увагу на загальний психологічний стан хворого, проводять опитування пацієнта щодо мотивації до харчування, виявляють можливі ознаки гіпотрофії як можливих наслідків тривалого обмеження стандартної дієти чи повної відмови від прийняття їжі |
Хворий вільно здійснює довільне ковтання |
5 |
|
Наявні незначні ускладнення при ініціації акту ковтання, але в цілому ковтання не порушене |
4 |
|
|
Хворому складно змусити себе ковтати, акт довільного ковтання супроводжується певними труднощами, з’являється відчуття страху (побоювання аспірації) |
3 |
|
|
Початок проведення акту ковтання пов’язаний зі значними зусиллями, хворий часто відмовляється від їжі (відчуття страху внаслідок високої вірогідності аспірації), наявні помірні ознаки гіпотрофії |
2 |
|
|
Хворий не може навіть розпочати акт ковтання, спостерігається значна гіпотрофія |
1 |
|
|
Сума балів |
||
Після завершення клінічного огляду та проведення бальної оцінки градацій кожної патологічної ознаки отримані бали підсумовують, загальна сума їх визначає функцію ротоглоткового статусу хворого та ступінь порушення акту ковтання в разі нейрогенної дисфагії.
Згідно з розробленою шкалою, значення сумарного балу клінічних проявів 7 свідчить про повну втрату функції ковтання (афагія); від 8 до 16 балів — про значні порушення ковтання; 17–25 балів — про помірні порушення; 26–32 бали — про незначні порушення функції ковтання; 33–35 балів — свідчать, що функція ковтання не порушена.
Порогові значення кількості балів для прийняття рішення щодо ступеня вираженості ротоглоткової дисфагії визначали, виходячи із теоретично очікуваного 5% (р<0,05) рівня помилкового віднесення до того чи іншого стану (Гублер Е.В., Генкін А.А., 1973).
Розроблений спосіб бальної діагностики та оцінки вираженості ротоглоткової дисфагії в гострий період мозкового інсульту опробований у неврологічному центрі Олександрівської клінічної лікарні м. Києва. Результати обстеження 65 пацієнтів після перенесеного гострого півкульного і стовбурового інсульту свідчать про різний ступінь дисфагічних порушень у пацієнтів з ротоглотковою дисфункцією: повну втрату функції ковтання з необхідністю зондового харчування — у 12,5% ; значні порушення ковтання — у 41,5%; помірні — у 35,4% і незначні дисфагічні розлади — у 10,8% випадків.
Цінність запропонованої методології оцінки ротоглоткової дисфагії визначається її простотою, неінвазивністю та можливістю здійснювати постійний моніторинг функції ковтання безпосередньо біля ліжка хворого в гострий період мозкового інсульту. Показник чутливості коливається від 80 до 85%.
Таким чином, математично-статистична обробка неврологічних функцій, пов’язаних з актом ковтання, дала можливість побудувати бальну систему оцінки нейрогенної дисфагії у хворих з гострим мозковим інсультом. Запропонована шкала дозволяє визначити тяжкість ротоглоткової дисфункції безпосередньо біля ліжка хворого, здійснювати постійний моніторинг ковтального статусу пацієнта, оцінювати ефективність застосованих реабілітаційних заходів.
ЛІТЕРАТУРА:
- Віничук С.М., Волосовець А.О.(2008а) Нейрогенна дисфагія в гострий період мозкового інсульту: фізіологія, патофізіологія, клінічні прояви та діагностика. Укр. мед. часопис, 3(65): 16–23(http://www.umj.com.ua/archive/65/pdf/649_ukr.pdf).
- Віничук С.М., Волосовець А.О.(2008б) Спосіб оцінки функції ковтання при нейрогенній дисфагії в гострий період мозкового інсульту. Патент на корисну модель № 32466 від 12.05.2008.
- Ворлоу Ч.П., Денниc М.С., Гейн Ж. и др.(1998) Инсульт: Практическое руководство для ведения больных. Политехника, СПб, 629 с.
- Генкин А.А., Гублер Е.В.(1964) Применение последовательного статистического анализа для дифференциальной диагностики и использование этого метода для различения двух форм ожоговой болезни. Применение математических методов в биологии и медицине. Л., Изд-во ЛГУ, Вып. I, с. 174–185.
- Гублер Е.В., Генкин А.А.(1973) Применение непараметрических критериев статистики в медико-биологических исследованиях. Л.: Медицина, 140 с.
- Aviv J.E., Kaplan S.T., Thomson J.E. et al.(2000) The safety of flexible endoscopic evaluation of swallowing with sensory testing(FEESST): an analysis of 500 consecutive evaluations. Dysphagia, 15(1): 39–44.
- Aviv J.E., Kim T., Sacco R.L. et al.(1998) FEESST: a new bedside endoscopic test of the motor and sensory components of swallowing. Ann. Otol. Rhinol. Laryngol., 107(5 Pt 1): 378–387.
- Bakheit A.M.(2001) Management of neurogenic dysphagia. Postgrad. Med. J., 77(913): 694–699.
- Buchholz D.W.(1993) Clinically probable brain stem stroke presenting primarily as dysphagia and nonvisualised by MRI. Dysphagia, 8(3): 235–238.
- Collins M.J., Bakheit A.M.(1997) Does pulse oximetry reliably detect aspiration in dysphagic stroke patients? Stroke, 28(9): 1773–1775.
- Daniels S.K., McAdam C.P., Brailey K. et al.(1997) Clinical assessment of swallowing and prediction of dysphagia severity. American Journal of Speech-Language Pathology, Vol. 6: 17–24.
- DePippo K.L., Holas M.A., Reding M.J.(1992) Validation of the 3-oz water swallow test for aspiration following stroke. Arch. Neurol., 49(12): 1259–1261.
- Ertekin C., Pehlivan M., Aydogdu I. et al.(1995) An electrophysiological investigation of deglutition in man. Muscle Nerve, 18(10):1177–1186.
- Ertekin C., Yüceyar N., Aydogdu І.(1998) Clinical and electrophysiological evaluation of dysphagia in myasthenia gravis. J. Neurol. Neurosurg. Psychiatry, 65(6): 848–856.
- Hila A., Castell J.A., Castell D.O.(2001) Pharyngeal and upper esophageal sphincter manometry in the evaluation of dysphagia. J. Clin. Gastroenterol., 33(5): 355–361.
- Holas M.A., DePippo K.L., Reding M.J.(1994) Aspiration and relative risk of medical complications following stroke. Arch. Neurol., 51(10): 1051–1053.
- Horner J., Massey E.W.(1988) Silent aspiration following stroke. Neurology, 38(2): 317–319.
- Logeman J.A.(1983) Evaluation and treatment of swallowing disorders. Austin, TX, Pro-ed.
- Mann G., Hankey G.J., Cameron D.(2000) Swallowing disorders following acute stroke: prevalence and diagnostic accuracy. Cerebrovasc. Dis.,10(5):380–386.
- Muz J., Mathog R.H., Hamlet S.L. et al.(1991) Objective assessment of swallowing function in head and neck cancer patients. Head Neck, 13(1): 33–39.
- Nathadwarawala K.M., Nicklin J., Wiles C.M.(1992) A timed test of swallowing capacity for neurological patients. J. Neurol., Neurosurg. Psychiatry, 55(9): 822–825.
- O’Donoghue S., Bagnall A.(1999) Videofluoroscopic evaluation in the assessment of swallowing disorders in paediatric and adult populations. Folia Phoniatr Logop., 51(4–5): 158–171.
- Ramsey D.J., Smithard D.G., Kalra L.(2003) Early assessments of dysphagia and aspiration risk in acute stroke patients. Stroke, 34(5): 1252–1257.
- Scott A., Perry A., Bench J.(1998) A study of interrater reliability when using videofluoroscopy as an assessment of swallowing. Dysphagia, 13(4): 223–227.
- Smithard D.G.(2002) Assessment of swallowing following stroke. Stroke Rev., 6: 7–10.
- Smithard D.G., O’Neill P.A., Park C. et al.(1998) Can bedside assessment reliably exclude aspiration following acute stroke? Age Ageing, 27(2): 99–106.
- Stanners A.J., Chapman A.N., Bamford J.M.(1993) Clinical predictors of aspiration soon after stroke. Age Ageing, 2(suppl. 2): A47.
- Tabaee A., Murry T., Zschommler A. et al.(2005) Flexible endoscopic evaluation of swallowing with sensory testing in patients with unilateral vocal fold immobility: incidence and pathophysiology of aspiration. Laryngoscope, 115(4): 565–569.
- Zaidi N.H., Smith H.A., King S.C. et al.(1995) Oxygen desaturation on swallowing as a potential marker of aspiration in acute stroke. Age Ageing, 24(4): 267–270.
- Zenner P.M., Losinski D.S., Mills R.H.(1995) Using cervical auscultation in the clinical dysphagia examination in long-term care. Dysphagia, 10(1): 27–31.
Резюме. Цель исследования — разработать неврологическую шкалу оценки ротоглотковой дисфункции у пациентов с нейрогенной дисфагией в острый период мозгового инсульта, используя связанные с нарушением функции глотания клинические критерии, методологию вероятностного анализа Байеса и алгоритм последовательной статистической процедуры Вальда — Генкина — Гублера. Обследовано 108 пациентов
с острым мозговым инсультом, среди которых 65 — с проявлениями нейрогенной дисфагии и 43 — без нарушения функции глотания. Для определения степени выраженности дисфагии была разработана неврологическая шкала оценки ротоглотковой дисфункции, которая основывалась на 7 достоверных клинических проявлениях, связанных с нарушением функции глотания. Разработанная шкала достаточно чувствительная и специфическая. Использование ее показало, что в острый период мозгового инсульта дисфагические нарушения бывают разной степени тяжести: полная потеря функции глотания с необходимостью зондового питания — у 12,5% пациентов; значительные нарушения глотания — в 41,5%; умеренные — в 35,4% и незначительные дисфагические расстройства — в 10,8% случаев.
Ключевые слова: нейрогенная дисфагия, диагностика,
клинические проявления, мозговой инсульт
Summary. The main aim of our research is to create neurological scale for evaluation of oropharyngeal dysfunction in acute stroke patients with neurogenic dysphagia, using clinical factors chained with swallowing dysfunction, method of Baies’s probability analysis and algorithm of subsequent statistical procedure of Wald — Hankin — Houbler. 108 acute stroke patients were examined. 65 patients had elements of neurogenic dysphagia and 43 were without swallowing disorders. We create a neurological scale for evaluation of dysphagia’s level, which is based on 7 most frequent clinical signs chained with impairment of swallowing function. This scale is adequately specific and sensitive. After evaluation of our group of acute stroke patients using developed scale we receive such clinical information: complete
loss of swallowing function was observed in 12.5%; severe disorders of deglutition — in 41.5%; average swallowing disorders — in 35.4% and light insignificant swallowing dysfunction — in 10.8% of cases.
Key words: neurogenic dysphagia, diagnostic assessment, clinical signs, stroke
Адреса для листування:
Волосовець Антон Олександрович
01601, Київ, бульв. Шевченка, 13
Національний медичний університет
імені О.О. Богомольця, кафедра неврології





