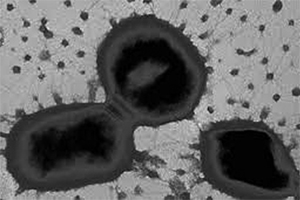
 Відомо, що у порожнині рота (ПР) налічується <700 видів бактерій, більшість з яких становить резидентну флору, яка стабілізує біоплівку ПР. Водночас підвищення рівня резидентної мікрофлори призводить до набуття нею вірулентності, а отже, зростання розвитку запальних процесів. До пародонтопатогенів належить близько 20 видів бактерій, які за ступенем вірулентності розподіляють на дві групи. До 1-ї групи належать бактерії, прямо пов’язані із прогресуванням захворювання, а до 2-ї групи — бактерії, що відіграють другорядну роль у розвитку захворювань пародонта. Porphyromonas gingivalis (P. gingivalis) належать саме до 1-ї групи (рисунок).
Відомо, що у порожнині рота (ПР) налічується <700 видів бактерій, більшість з яких становить резидентну флору, яка стабілізує біоплівку ПР. Водночас підвищення рівня резидентної мікрофлори призводить до набуття нею вірулентності, а отже, зростання розвитку запальних процесів. До пародонтопатогенів належить близько 20 видів бактерій, які за ступенем вірулентності розподіляють на дві групи. До 1-ї групи належать бактерії, прямо пов’язані із прогресуванням захворювання, а до 2-ї групи — бактерії, що відіграють другорядну роль у розвитку захворювань пародонта. Porphyromonas gingivalis (P. gingivalis) належать саме до 1-ї групи (рисунок).
Згідно зі статистичними даними, захворюваність на пародонтит, який, як відомо, є основною причиною втрати зубів, становить приблизно 10,0–17,6% і найчастіше супроводжується підвищенням рівня запальних факторів. Патогенні мікроорганізми, пов’язані з розвитком різних системних захворювань, включаючи онкозахворювання, можуть поширюватися кровоносними судинами та інфікувати навіть головний мозок внаслідок анатомічної спорідненості. Вченими встановлена певна залежність між втратою зубів та ризиком розвитку раку шлунково-кишкового тракту (ШКТ), яка виражається співвідношенням доза–ефект. Зокрема, загальний ризик розвитку раку підвищується на 9% на кожні 10 втрачених зубів, на 14% зростає ризик розвитку раку стравоходу, на 9% — раку шлунка, на 31% — раку голови та шиї, на 4% — колоректального раку та на 7% — раку підшлункової залози.

P. gingivalis є важливою патогенною бактерією, яка опосередковує місцевий запальний процес у пародонті з подальшою її адгезією та проникненням у глибші структурні елементи пародонта. При цьому відбувається порушення нормального фізіологічного метаболізму та пригнічення активації апоптозу протеаз, які належать до потенційних факторів ризику розвитку раку. Розвиток неопластичних процесів ШКТ характеризується високим ступенем коморбідності та смертності на тлі незадовільного рівня ранньої діагностики та високої вартості лікування. P. gingivalis, що виявляється у пародонтальних кишенях, є грамнегативним облігатним анаеробом, здатним експресувати специфічні фактори вірулентності, включаючи триходерму, гінгіпаїни, білок послідовності тетратрикопептидного повтору, позаклітинні полісахариди, систему поглинання гемоглобіну, ліпополісахариди тощо. Коактивація гінгіпаїнів із ліпополісахаридами впливає на порушення функцій імунного захисту тканин пародонта та спричиняє розвиток запалення, деструкцію періодонта і кістки.
Гінгіпаїни здатні руйнувати чужорідні білки та поліпептиди, необхідні для живлення та росту власне P. gingivalis. Будучи внутрішньоклітинною патогенною бактерією, P. gingivalis здатна проникати до різних еукаріотичних клітин, таких як ендотеліальні клітини аорти та коронарної артерії, а також до ендотеліальних клітин пупкової вени, епітеліальних клітин ясен, гладких м’язів коронарної артерії, епітеліальних букальних клітин. Після інвазії бактерія змінює спрямованість експресії, щоб запобігти імунній відповіді хазяїна. Подальша колонізація слугує потенційно небезпечним резервуаром для майбутньої реінфекції.
P. gingivalis і плоскоклітинний рак ПР
Рак ПР — найпоширеніший різновид раку у світі з максимальною розповсюдженістю у країнах, що розвиваються. Захворювання характеризується високою частотою рецидивування та несприятливим прогнозом. Пацієнти скаржаться на наявність логопатії та дисфагії. Конкретні фактори ризику, що спричиняють розвиток такого загрозливого стану, включають шкідливі харчові звички, тютюнопаління, алкоголізм, наявність вірусу папіломи людини високого канцерогенного ризику та генетичну схильність. Проте у 15% пацієнтів виникнення плоскоклітинного раку ПР не обмежується тільки цими факторами.
P. gingivalis і рак стравоходу
Гістологічно рак стравоходу включає аденокарциному стравоходу та плоскоклітинний рак; при цьому поширеність аденокарциноми переважає серед населення західних країн, а плоскоклітинного раку — серед населення східних країн. Вважається, що P. gingivalis є домінуючим фактором, що бере участь у канцерогенезі епітелію стравоходу.
P. gingivalis та рак шлунка
Рак шлунка посідає четверте місце у структурі онкопатології. Результати метааналізів продемонстрували, що втрата зубів підвищує ризик розвитку неопластичного процесу. Колонізація патогенами пародонта пов’язана з підвищеним ризиком розвитку передракових захворювань шлунка, що дозволяє припустити асоціацію між рівнем їх колонізації та розвитком раку шлунка.
- Liu X., Gao Z., Sun C. et al. (2019) The potential role of P.gingivalis in gastrointestinal cancer: a mini review (https://infectagentscancer.biomedcentral.com/articles/10.1186/s13027-019-0239-4).
Катерина Приходько-Дибська





