ВВЕДЕНИЕ
Гигантские аневризмы головного мозга представляют самостоятельную группу внутричерепных мешотчатых аневризм не только в силу своего размера (свыше 2,5 см в диаметре), но и благодаря особенностям клинического течения, диагностики и сложности нейрохирургического лечения. Они составляют около 10% всех внутричерепных аневризм (Лазарев В.А., 1995; Лебедев В.В. и соавт., 1996; Adams W.M. et al., 2000; Lownie S.P. et al., 2000).
Показатели, обеспечивающие эффективность хирургического лечения, гигантских аневризм головного мозга, — ранняя диагностика, углубленное обследование состояния больного, изучение топографо-анатомических особенностей строения сосудов основания головного мозга, дифференцированный подход к выбору метода хирургического лечения, определения его этапности и последовательности.
Основным методом диагностики гигантских артериальных аневризм головного мозга остается обычная церебральная ангиография (ЦАГ). Ангиографически выделяют две формы гигантских аневризм — нетромбированная и тромбированная. В 85% случаев истинные размеры аневризмы определяются во время операции или секции.
При компьютерной томографии (КТ) головного мозга в типичных случаях гигантские аневризмы представляются образованием округлой или овальной формы с четкими границами (Лебедев В.В. и соавт., 1996; Steinman D.A. et al., 2003). Сочетанное использование ЦАГ и КТ головного мозга позволяет диагностировать гигантскую аневризму практически в 100% случаев (Ciceri E.F. et al., 2001).
С помощью трехмерной (3Д)-КТ можно получить точную информацию о размерах и анатомических взаимоотношениях шейки аневризмы и несущей артерии и окружающих ветвей (Черемисин В.М. и соавт., 2002).
В связи с риском развития ишемических осложнений после операции (Лазарев В.А., 1995; Коновалов А.Н. и соавт., 1997; Труфанов Г.Е. и соавт., 2006) предоперационная оценка функциональной значимости мозговых сосудов должна быть составной частью диагностического процесса у больных с гигантскими аневризмами.
На принципе кратковременного выключения кровотока в магистральном сосуде основана проба Матаса, применяющаяся для оценки состояния коллатерального кровообращения путем сдавления внутренней сонной артерии на шее. Этот тест нетрудоемкий, безопасный и информативный. Поэтому его стали использовать для оценки состояния коллатерального кровообращения головного мозга у нейрохирургических больных (Беличенко О.И. и соавт., 1998; Гайдар Б.В. и соавт., 2000; Lownie S.P. et al., 2000; Гайдар Б.В., 2002; Steinman D.A. et al., 2003).
Недостаточность мозгового кровообращения приводит к нарушению тканевого ионного баланса, поэтому об ее развитии можно судить по электрофизиологическим изменениям и, в частности, по данным электроэнцефалографии (ЭЭГ), мониторингу вызванных потенциалов (Steinman D.A. et al., 2003).
В последние годы широкое распространение получила транскраниальная ультразвуковая допплерография головы (ТКУЗДГ). По мнению многих авторов неинвазивное измерение линейной скорости и направления кровотока в мозговых сосудах до и во время компрессионных проб позволяет оценить состояние коллатерального кровотока мозга (Тиссен Т.П. и соавт., 2001; Свистов Д.В. и соавт., 2002).
Методом оценки коллатерального мозгового кровообращения является и контралатеральная каротидная ангиография в условиях временной окклюзии исследуемого магистрального сосуда. О состоянии коллатерального кровообращения при этом судят по степени контрастирования соединительных артерий и сосудов контралатеральной артерии, а также дистальных отрезков окклюзированного сосуда (Гайдар Б.В. и соавт., 2000). Таким образом, для мониторинга адекватности мозгового кровообращения наибольший интерес представляют прямые количественные способы измерения мозгового кровотока для определения допустимости выключения артерии, несущей аневризму.
Цель работы — определить оптимальную последовательность диагностических мероприятий (ЦАГ, КТ, компьютерная томографическая ангиография (КТ-АГ), магнитно-резонансная томография (МРТ), магнитно-резонансная томографическая ангиография (МРТ-АГ) головного мозга, ТКУЗДГ, ЭЭГ) и установить диагностическую ценность каждого метода при данной патологии.
ОБЪЕКТ И МЕТОДЫ ИССЛЕДОВАНИЯ
В работе проведен анализ комплексного обследования 89 больных с гигантскими аневризмами головного мозга, находившихся на обследовании и лечении в Институте нейрохирургии им. А.П. Ромоданова АМН Украины в 1998–2006 гг.
Во всех наших наблюдениях один из размеров аневризмы обязательно превышал 2,5 см.
Основная группа включает больных в возрасте от 30 до 59 лет — 67 (75,3%). Самому младшему пациенту было 13 лет, самому старшему — 78 лет. Многочисленной оказалась группа в возрасте 40–49 лет — 29 (32,3%).
Большинство больных женщины — 56 (63%), мужчины — 33 (37%). Наиболее часто встречались аневризмы внутренней сонной артерии — у 49 (55%) больных. У 4 (4,5%) больных аневризма располагалась в вертебробазилярном бассейне.
Из 89 больных, поступивших в стационар вне геморрагического периода, у 48 (54%) — аневризмы протекали по псевдотуморозному типу, а у 41 (46%) — внутричерепное кровоизлияние произошло ранее чем за месяц до госпитализации.
Диагностический комплекс включал клинико-неврологическое и офтальмологическое исследования, КТ, КТ-АГ, МРТ, МРТ-АГ головного мозга, ЦАГ, ЭЭГ, ТКУЗДГ.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Диагностика гигантских аневризм заключается в определении несущего аневризму сосуда, локализации и размеров аневризмы, уточнения ее строения (расположение и размер шейки, толщина стенок аневризмы, степень тромбирования и т.д.). Кроме того, необходимо выяснить состояние коллатерального кровообращения головного мозга в бассейне несущей аневризму артерии. Для диагностики гигантских аневризм большое значение имеет КТ головного мозга, которая была проведена всем 89 больным. Аневризма видна даже на снимках, полученных без контрастного усиления (рис. 1, 2), но применение последнего дает возможность получить более четкое изображение самой аневризмы и дифференцировать ее с опухолями мозга.

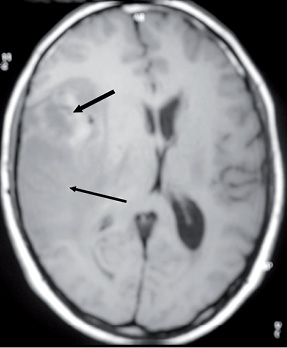
У всех больных, поступивших на острой стадии кровоизлияния, с помощью КТ выявили разрыв аневризмы с субарахноидальным или паренхиматозным кровоизлиянием, определили степень ее тромбирования и состояние стенок, что позволило спланировать тактику лечения.
Частота тромбирования гигантских аневризм составила 73 (82%) случая. Для них была характерна «толстая» стенка и пристеночное тромбирование значительной части аневризмы.
Важное диагностическое значение представляет трехмерная КТ-реконструкция (SSD — Shaded Surface Display/метод оттененных поверхностей) (проводили у 8 больных), дающая объемную пространственную информацию, позволяющую определить соотношение донорского сосуда и аневризматического мешка (рис. 3). КТ в раннем послеоперационном периоде важна для контроля за состоянием мозгового вещества (отек, ишемия) и исключения послеоперационной гематомы.

МРТ проведена всем 89 больным. Она характеризуется более высокими разрешающими способностями, особенно при проведении дифференциального диагноза между аневризмой и различными объемными процессами. Она позволяет получить информацию, практически равноценную ЦАГ. Особую важность представляет трехмерная (3D) МРТ-реконструкция (проводили у 8 больных), дающая объемную пространственную информацию, что позволяло определить соотношение ветвей магистрального сосуда головного мозга и аневризматического мешка.



При наличии артериального тромба, особенно при гигантских аневризмах, определяется зона так называемой «слойности» МРТ-сигнала, который формируется за счет участков трансформации гемоглобина на разных стадиях тромбоза. На периферии гигантских тромбированных аневризм во всех случаях определялась фиброзная капсула с гемосидерином либо отложениями извести.
МРТ-АГ производили в комплексе с МРТ в режиме, оптимальном для визуализации нетромбированных аневризм. МРТ-АГ обследование проводили у 38 больных.
После установления размеров и локализации аневризмы исключительно важным являлось исследование функционального состояния коллатерального кровообращения.
Для оценки адекватности коллатерального кровообращения до операции производилась ЭЭГ во время пальцевого сдавления общей сонной артерии на шее на одноименной поражению стороне (проба Матаса). Всего до операции по схеме «ЭЭГ + тест Матаса» нами обследовано 58 больных. На основании анализа полученных данных отмечались следующие три формы компенсации коллатерального кровообращения головного мозга:
1. Компенсированная форма — отсутствие локальных изменений на ЭЭГ, нарастание признаков раздражения подкорково-диэнцефальных структур. Такая форма коллатерального кровообращения обнаружена у 48 (82,7%) больных. У этих больных по данным АГ и ТКУЗДГ наблюдалось анатомически нормальное строение Виллизиева круга.
2. Субкомпенсированная форма — наличие диффузных изменений на ЭЭГ в виде преобладания частых форм активности без локальных признаков. В эту подгруппу вошли 10 (17,3%) больных.
3. Декомпенсированная форма — наличие значительных изменений на ЭЭГ в виде генерализованных медленных волн на стороне патологии и клинических признаков ишемии. В нашем наблюдении больных с этой формой не было.
ТКУЗДГ производилась транскраниальным методом с использованием сканирующого прибора «Siemens Sonoline 650». Регистрировалась линейная скорость кровотока и его направление в отделах мозговых артерий. Определение этих показателей и их изменений на фоне компрессионных проб позволяло с определенной степенью достоверности судить о состоянии коллатерального кровоснабжения по соединительным артериям и каротидно-офтальмическому анастомозу. Последнее особенно важно при аневризмах внутренней сонной артерии, когда оценка функции указанного анастомоза позволяет прогнозировать состояние коллатерального кровоснабжения при окклюзии внутренней сонной артерии.
Адаптационные способности коллатерального кровообращения головного мозга путем изучения динамики мозгового кровотока при пережатии сонной артерии на стороне аневризмы проведены у 53 больных. Определялась скорость кровотока по СМА на стороне аневризмы по сравнению с интактной стороной и реакция кровотока в СМА на компрессию одноименной сонной артерии на шее. В зависимости от степени снижения скорости кровотока по СМА при компрессии сонной артерии исследованные больные были разделены на две группы:
Первая группа — с хорошим коллатеральным кровообращением. В эту группу вошли 38 (71,7%) пациентов, у которых при компрессии сонной артерии на шее отмечалось незначительное снижение скорости кровотока (на 30–40%).
Вторая группа — с плохим коллатеральным кровообращением. В данной группе было 15 (28,3%) больных, у которых отмечалось более существенное снижение скорости кровотока (на 60–70%).
Для объективизации проба Матаса сочеталась либо с одновременной ТКУЗДГ, либо с записью ЭЭГ до, на фоне пробы и после нее. Исследования по схеме «ЭЭГ + проба Матаса» и «ТКУЗДГ + проба Матаса» проведены у 53 больных с аневризмами внутренней сонной артерии. Было выявлено, что появление изменений на ТКУЗДГ и ЭЭГ во время пробы и их исчезновение по окончанию коррелируют с одновременной динамикой неврологических симптомов и свидетельствуют о недостаточности перетока по соединительным артериям.
Решающее значение в диагностике гигантских артериальных аневризм головного мозга принадлежит ЦАГ. Исследовалось 89 больных. Наряду с подтверждением диагноза внутричерепной аневризмы получены сведения о размерах полости аневризмы, особенностях отношения шейки аневризмы к донорскому сосуду, состоянии Виллизиева многоугольника и некоторых особенностях мозгового кровообращения. Суждения об истинных размерах гигантской аневризмы головного мозга по ангиограммам относительны, так как у большей части больных ее полость частично тромбирована (рис. 7). Признаками частичного тромбирования гигантских артериальных аневризм на ангиограммах были неровности контуров полости, дефекты ее наполнения, смещение близлежащих сосудов.

Размеры шейки аневризмы в сравнении с диаметром донорского сосуда приведены в табл. 1.
| Размеры шейки аневризмы | Количество больных | % |
|---|---|---|
| Шейка узкая | 23 | 25,8 |
| Шейка широкая | 66 | 74,2 |
| Всего | 89 | 100 |
Шейку аневризмы считали узкой, если ее диаметр составлял не более половины диаметра донорского сосуда, широкой — если он был близок к нему. Широкая шейка аневризм выявлена у 66 (74,2%) больных (рис. 8). У остальных 23 (25,8%) она была узкой. Из приведенных данных видно, что у больных с гигантскими аневризмами чаще встречаются аневризмы с широкой шейкой.

При ангиографии, оценивая анатомическую состоятельность артериального круга мозга, мы выделяли два его варианта: типично сформированный (хорошее развитие передней и задней соединительных артерий) и нетипично сформированный артериальный круг мозга (недоразвитие или отсутствие одной или нескольких соединительных артерий).
Особенности строения Виллизиева круга кровообращения представлены в табл. 2. У 63 (70,8%) пациентов были выявлены признаки типично сформированного артериального круга, что свидетельствует о возможности выключения гигантской аневризмы вместе с несущей ее артерией.
| Виллизиев круг | Количество больных | % |
|---|---|---|
| Типично сформированный | 63 | 70,8 |
| Нетипично сформированный | 26 | 29,2 |
| Всего | 89 | 100 |
Однако для решения вопроса об адекватности коллатерального кровотока в случае выключения несущего аневризму сосуда данных ЦАГ не всегда есть достаточным и требует проведения дополнительных исследований: проба Матаса, ЭЭГ и ТКУЗДГ.
ВЫВОДЫ
Полученные и оцененные нами данные исследований позволяют сделать вывод, что формулирование хирургического диагноза «гигантская мешотчатая аневризма мозга» требует оценки не только ее топографо-анатомических особенностей и варианта течения заболевания, но и тщательного изучения возможностей коллатерального кровоснабжения различных отделов мозга. Самым информативным и адекватным методом исследования коллатерального кровотока следует признать ангиографическое обследование, которое может дополняться объективным контролем методами ЭЭГ, ТКУЗДГ с применением компрессионного теста.
ЛИТЕРАТУРА
- Беличенко О.И., Дадвани С.А., Абрамова Н.Н., Терновой С.К. (1998) Магнитно-резонансная томография в диагностике цереброваскулярных заболеваний. Видар, Москва, 111 с.
- Гайдар Б.В. (ред.) (2002) Практическая нейрохирургия. Руководство для врачей. Гиппократ, Санкт-Петербург, 648 с.
- Гайдар Б.В., Парфенов В.Е., Свистов Д.В. (2000) Транскраниальная допплерография в нейрохирургии. Санкт-Петербург, 69 с.
- Коновалов А.Н., Корниенко В.Н., Пронин И.Н. (1997) Магнитно-резонансная томография в нейрохирургии. Видар, Москва, 471 с.
- Лазарев В.А. (1995) Клиника, диагностика, хирургическое лечение крупных и гигантских мешотчатых аневризм головного мозга: Автореф. Дис. … д-ра мед. наук. Москва, 24 с.
- Лебедев В.В., Крылов В.В., Шелковский В.Н. (1996) Клиника, диагностика и лечение внутричерепных артериальных аневризм в остром периоде кровоизлияния. Москва, 146 с.
- Свистов Д.В., Кандыба Д.В., Савелло А.В. и др. (2002) Современное состояние церебральной ангиографии и ее место в комплексе методов диагностики сосудисто-мозговых заболеваний. Материалы III съезда нейрохирургов России. Санкт-Петербург, С. 674–675.
- Тиссен Т.П., Пронин И.Н., Белова Т.В. (2001) Возможности спиральной компьютерной томографии в нейрохирургии. Нейрохирургия, 1: 14–18.
- Труфанов Г.Е., Рамешвили Т.Е., Фокин В.А., Свистов Д.В. (2006) Лучевая диагностика сосудистых мальформаций и артериальных аневризм головного мозга. Элби-СПб, Санкт-Петербург, 224 с.
- Черемисин В.М., Труфанов Г.Е., Зейдлиц В.Н., Кандыба Д.В. (2002) Магнитно-резонансная томография и магнитно-резонансная ангиография головного мозга в норме. Воен.-мед. акад., Санкт-Петербург, 19 с.
- Adams W.M., Laitt R.D., Jackson A. (2000) The role of MR angiography in the pretreatment assessment of intracranial aneurysms: a comparative study. AJNR Am. J. Neuroradiol., 21(9): 1618–1628.
- Ciceri E.F., Klucznik R.P., Grossman R.G., Rose J.E., Mawad M.E. (2001) Aneurysms of the posterior cerebral artery: classification and endovascular treatment. AJNR Am. J. Neuroradiol., 22(1): 27–34.
- Lownie S.P., Drake C.G., Peerless S.J., Ferguson G.G., Pelz D.M. (2000) Clinical presentation and management of giant anterior communicating artery region aneurysms. J. Neurosurg., 92(2): 267–277.
- Steinman D.A., Milner J.S., Norley C.J., Lownie S.P., Holdsworth D.W. (2003) Image-based computational simulation of flow dynamics in a giant intracranial aneurysm. AJNR Am. J. Neuroradiol., 24(4): 559–566.
ДІАГНОСТИКА ГІГАНТСЬКИХ МІШКОПОДІБНИХ АНЕВРИЗМ АРТЕРІЙ ГОЛОВНОГО МОЗКУ
Резюме. Наразі для діагностики гігантських артеріальних аневризм головного мозку застосовують дослідження колатерального кровообігу методом церебральної ангіографії, яку можуть доповнювати методи об’єктивного контролю — електроенцефалографія, транскраніальна ультразвукова допплерографія голови з застосуванням компресійного тесту. Це має вирішальне значення для вибору найбільш адекватного методу хірургічного лікування.
Ключові слова:гігантська мішкоподібна аневризма, методи діагностики, ангіографія, колатеральне кровопостачання
DIAGNOSTICS OF THE GIANT SACCULAR CEREBRAL ANEURYSMS
Summary. Nowadays, the method of collateral blood supply examination with cerebral angiography is used for the giant cerebral aneurysms diagnostics, which may be supplemented with other objective methods — electroencephalography and transcranial ultrasound dopplerography with compression test. It has a decisive importance for the choice of the most adequate surgical treatment.
Key words: giant aneurism, diagnostic methods, angiography, collateral blood supply
Адрес для переписки:
Хиникадзе Мирза Резоевич
04050, Киев, ул. Мануильского, 32
Институт нейрохирургии им. А.П. Ромоданова АМН Украины
E-mail: [email protected]





